欢迎光临吉康旅!
美国食品和药物管理局批准达克替尼(辉瑞制药)用于一线治疗。 FDA批准检测转移性非小细胞肺癌患者表皮生长因子受体(EGFR)外显子19缺失或外显子21替代突变()。
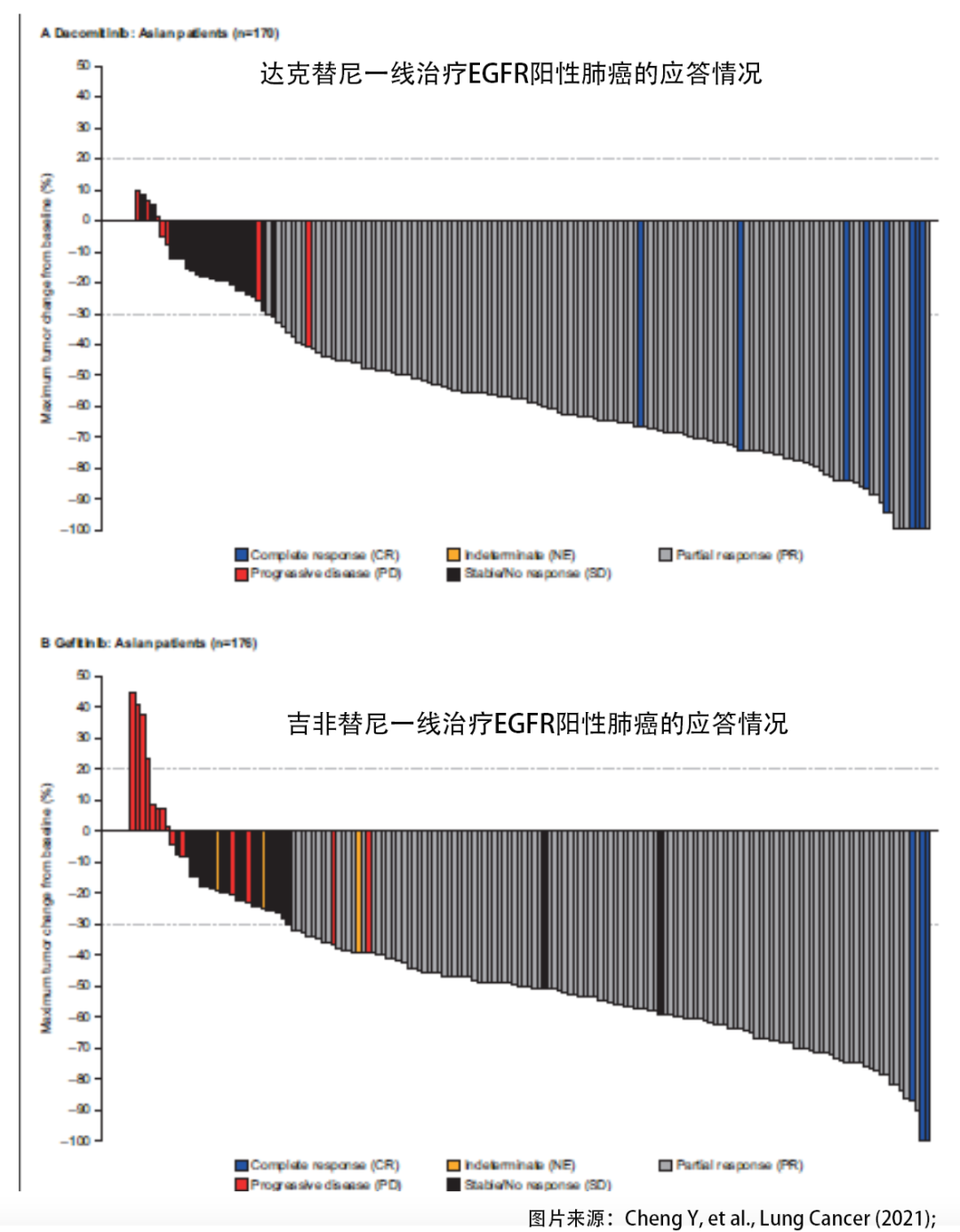
该批准基于一项随机、多中心、开放标签活性对照试验 (1050;),该试验比较了达克替尼和吉非替尼在 452 名不可切除转移患者中的安全性和有效性。要求患者既往无转移性疾病或复发性疾病治疗,且在完成全身非EGFR TKI治疗后至少有12个月的无病期;东方肿瘤合作组织的绩效状态为0或1;和 EGFR No. 19 外显子缺失或外显子 21 替换突变。患者被随机分配(1:1) 每天一次口服达克替尼 45 mg,或每天口服一次吉非替尼 250 mg,直到疾病进展或出现不可接受的毒性。
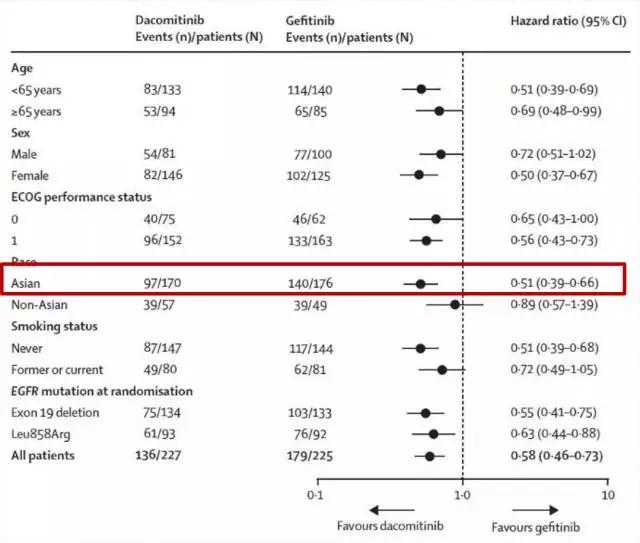
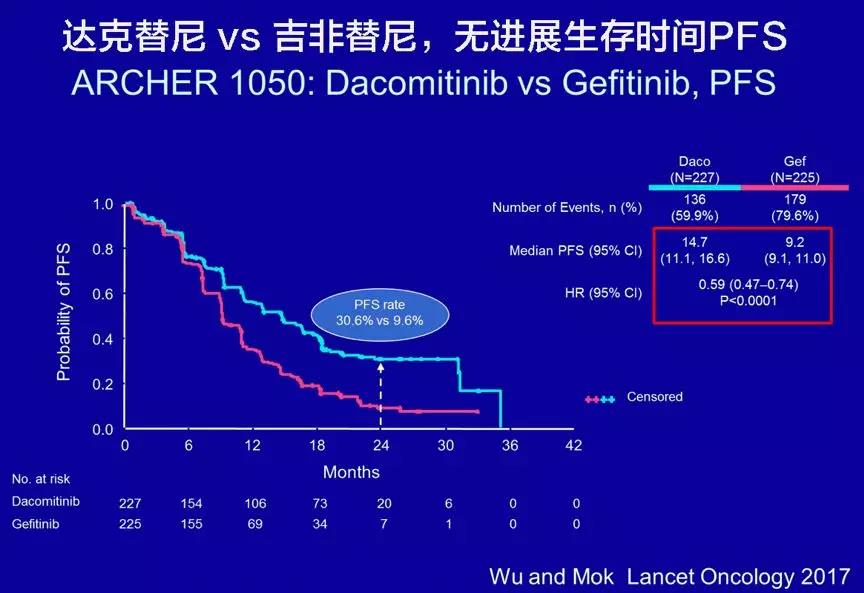
试验表明,无进展生存期(肿瘤在药物控制下重新生长所需的时间)得到了显着提高;总体反应率或总体生存率没有改善。独立审查委员会确定达克替尼组和吉非替尼组的中位无进展生存期分别为14.7和9.2个月(风险比0.59;95%CI:0.47,0.74;达克替尼最常见(>20%)的不良反应是腹泻、皮疹、骨刺、口腔炎、食欲下降、皮肤干燥、体重减轻、脱发、咳嗽和瘙痒)。达克替尼的推荐剂量为 45 mg,每天一次,有或没有食物。如有需要,请咨询康必星海外医疗医疗顾问:或扫描二维码添加以下微信,我们将竭诚为您服务!
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话
BottinibCabozantinib在脑转移肾细胞癌中表现出怎样的治疗效果?
2022-09-22奥拉帕利靶向药的适用卵巢癌类型,奥拉帕利用于卵巢癌化疗维持治疗的适应症
2022-09-22MET是一种由MET基因编码的受体酪氨酸激酶,许多癌症与MET受体途径的异常信号有关。METex14是一种公认的致癌驱动因素,在新诊断的晚期非小细胞...
在真实世界中,阿比特龙对转移性激素敏感性前列腺癌(mHSPC)患者中展现出了良好的疗效。以下是一例来自临床的经典案例:患者跳过化疗直接...
脑转移治疗的金标准是局部治疗,包括立体定向放射外科治疗、全脑放疗和外科手术治疗。脑转移RCC患者的体力状态较差,且通常需马上进行局...
奥拉帕利(利普卓)在卵巢癌共获批四大适应症,维持和挽救两种用法:①单药用于BRCA1/2胚系和体系突变,一线含铂化疗后达到CR/PR晚期卵巢...
4项不同研究分析数据证实,Vitrakvi(拉罗替尼)对携带NTRK融合基因的实体瘤(也称为TRK融合肿瘤)患者有持续临床获益。结果已在2021年9...








