欢迎光临吉康旅!
原文链接:
-3(GPC3)基因位于染色体Xq26,主要编码580个氨基酸的Da前体核心蛋白,又称DGSX,GTR2-2、MXR7、OCI-5等,该蛋白可裂解为40 000 Da N端蛋白和C端蛋白,可被单克隆抗体识别。GPC3是硫酸乙酰肝素糖蛋白( )家族的成员,由糖基磷脂酰肌醇( GPI) 锚点附着在细胞膜上,在人类胚胎中广泛表达。GPC3 可通过胰岛素样生长因子、骨相关形态发生蛋白、成纤维细胞生长因子 (FGF) 或 -hog 信号传导调节细胞形态发生和生长,以及与多种细胞表面相互作用。受体的相互作用调节其下游信号通路,从而调节细胞粘附、增殖、分化、侵袭和迁移等生物学行为。
GPC3在多种实体瘤中高表达,而在正常成人组织中含量极低,有望成为多种实体瘤的治疗靶点。在成人组织中,GPC3 仅在心脏、肺、肾和卵巢中低表达,在骨骼肌、胰腺、小肠和结肠中表达最低。同时,GPC3在肿瘤组织中的表达存在差异:在肝癌(HCC)、非小细胞肺癌、睾丸和卵巢卵黄囊瘤、恶性黑色素瘤、卵巢透明细胞癌(OCCA)、特殊型胃癌中(GC)、ESCC、睾丸生殖细胞肿瘤、结肠癌、肾横纹肌瘤,但在卵巢癌、胆管癌、GC 和间皮瘤中下调,被认为是这些肿瘤中的抑制基因。
近年来,国际上很少有肝癌靶向药物获批上市,许多III期临床研究以失败告终。异质性被认为是肿瘤无法治愈的主要原因,而肝癌是异质性最强的恶性肿瘤之一。由于肝癌的高异质性,目前尚未发现相关的“癌基因依赖”,因此分子靶向治疗效果甚微。其中,HCC约占所有肝癌的90%。根据 & 的数据,2019 年全球 HCC 患者人数达到 77.60,000 人,预计 2024 年将增加到 87.660,000 人,到 2030 年将增加到 100 人。 2024 年至 2030 年的年增长率为 2.3%。我国是肝癌高发国家,45%以上的肝癌病例来自中国。2019年我国HCC患者达到36.94万,预计2024年增加到41.65万,2030年增加到47.34万。复合增长率从2024 年到 2030 年是 2.2%。目前HCC的治疗水平有了很大提高,从传统的化疗到多激酶抑制剂和检查点抑制剂治疗,但整体的治疗选择仍然非常有限,特别是对于晚期肝癌患者,只有少数二- 线和后续治疗选项。因此,晚期HCC患者仍有巨大的未满足的临床需求。研究表明,GPC3 是 HCC 的可靠标志物,可辅助确认HCC早期病变的性质,可显着提高诊断的准确性。此外,基于GPC3靶点的治疗策略主要集中在抗体药物、细胞治疗和疫苗[1-3]。
一、最新研究进展
1、据不完全统计,目前在研的GPC3药物有38个,其中II期1个,I/II期5个,I期17个,临床应用1个,临床前片14个。2、在研公司及适应症:其中科济药业在研,罗氏在研3家,药明康诺在研2家,在研2家,(NIH)在研2家,康诺亚生物在研1、在研1、在研1、益妙神舟在研1。适应症主要是实体瘤,尤其是肝细胞肿瘤。
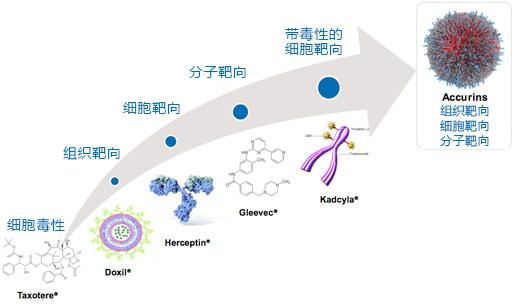
3、临床阶段以上药物及其作用机制统计如下:
二、重点药品及企业介绍
1、GPC3 抗体
作为创新靶点,GPC3的研发管线并不拥挤,绝大多数单抗仍处于临床前阶段。罗氏中外药业的(GC33))是首个靶向GPC3的抗体,目前处于临床II期。然而,GC33的临床之路并不平坦,屡屡遭遇滑铁卢。肝细胞癌患者疗效的 II 期临床试验显示 GC33 和安慰剂之间的总生存期和无进展生存期没有显着差异。与安慰剂相比,GC33 的 mPFS 为 2. 6 个月 vs 1.5 个月,mOS 为 8.7 个月 vs 10 个月。然而,该临床亚组分析的结果表明,GC33可以改善GPC3过表达肝细胞癌患者的预后。
此外,中外药业还在GC33的基础上开发了靶向CD3/GPC3的双特异性抗体,即。该抗体有2个不同的可变区,其中一个识别肿瘤抗原GPC3,另一个用于结合表达CD3抗原的T细胞。双特异性抗体构成T细胞和肿瘤细胞之间的免疫突触,将T细胞募集到肿瘤部位,从而激活T细胞免疫机制,并介导T细胞杀死过表达GPC3的肿瘤细胞。在剂量递增I期试验中,共有29名受试者入组,剂量范围为0.003-0.81μg/kg。结果显示,超过20%的患者出现CRS反应和发热。0.81μg/kg的剂量被证明是不能耐受的;当剂量低于0.81μg/kg时,耐受性好,激素和抗IL-6R治疗后毒副作用可控。近日,一项新的I期临床研究评估了(PD-L1)和贝伐单抗(VEGF)联合治疗晚期肝细胞癌患者)的安全性、耐受性和初步疗效数据,患者目前正在招募。
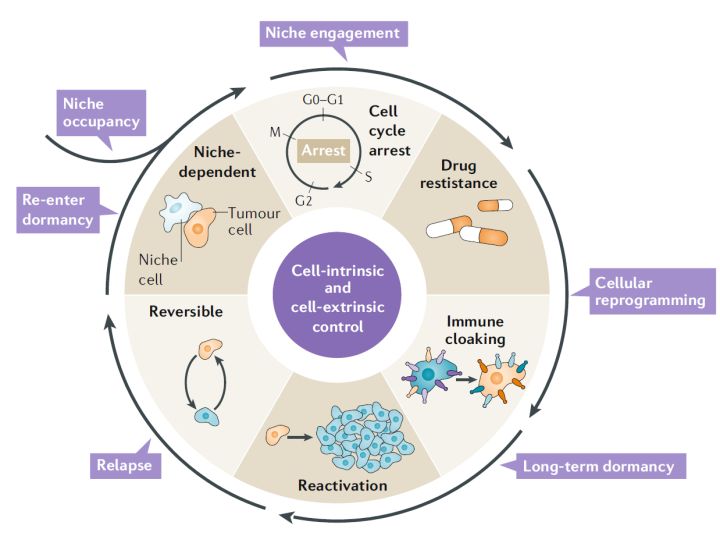
2、CAR-T
是公司领先的 CAR-T 项目,用于治疗各种表达 GPC3 的实体瘤。它基于专有的 BOXR™ 平台,旨在提高 T 细胞在恶劣的肿瘤微环境中的适应性。与传统的 GPC3 CAR-T 细胞相比,在缺氧和低葡萄糖条件下,临床前研究已经确定了“螺栓固定”转基因的作用机制并证明了对抑制性肿瘤微环境的抗性。显示 T 细胞增殖得到改善,具有更好的肿瘤杀伤能力;此外,与对照细胞相比,从动物身上分离的肿瘤浸润淋巴细胞对功能障碍的抵抗力更强,衰竭标志物更少。 的临床研究计划预计将于 2022 年初开始。2021 年 12 月,
科际药业的在研产品有两款靶向GPC3的CAR-T治疗产品,分别为和,均已进入I期临床试验。其中,治疗GPC3阳性实体瘤的临床试验申请于2019年获得国家CDE批准,2020年将公布临床结果,是全球首个靶向GPC3 CAR-T细胞治疗的药物肝细胞癌。该研究是在手术治疗、局部治疗或全身治疗后疾病进展的患者中进行的。临床结果显示,半年、1年、3年生存率分别为:50.3%、42.0%、10.5%;PR(部分缓解)率为15%(2例),2例患者生存时间分别为20.5个月和44. 2个月; 中位生存期为 278 天。在安全性方面,分别有 13、12 和 9 名患者出现发热、淋巴细胞计数下降和 CRS;8 例患者出现 1/2 级 CRS 反应,1 例患者出现 5 级 CRS 反应;没有患者有 5 级 CRS 反应。发生 3/4 级神经毒性。这一结果表明,科基生物的靶向GPC3的CAR-T疗法在人体内是安全可控的,对晚期肝细胞癌患者已显示出一定的疗效。基于新一代CAR-T技术平台,体内结果显示,在3个小鼠实体瘤模型(胰腺癌、乳腺癌和肝癌)和未经环磷酰胺预处理的情况下,与传统的CAR-T T细胞或IL- 7/共表达的CAR-T细胞表现出更显着的功效。IL-7并能提高CAR-T细胞和DC细胞在肿瘤中的存活和浸润;免疫组化证实对肿瘤血管生成有抑制作用。
吉凯基因也在开发针对 GPC3 的 CAR-T 疗法,目前正在进行探索性临床 I/II 期研究。截至目前,吉凯基因尚未向CDE提交临床申请。除了科际药业和吉凯基因外,华夏盈泰、北京益妙、恒润大生、上海医药、亚伯药业和元启生物都在研发GPC3靶向CAR-T疗法。有望在GPC3领域取得突破。
外表
虽然GPC3在HCC发生发展中的作用机制尚不完全清楚,但其对HCC诊断和治疗的影响已被揭示。在病理诊断方面,GPC3是诊断HCC的可靠指标之一;作为HCC分子靶向治疗的靶点,GPC3将为HCC的治疗开辟一条新途径。相信随着对GPC3分子作用机制研究的深入,其应用前景将更加广阔。
参考
[1]冯敏,何敏-3:一作[J]。FEBS, 2014, 588(2): 377-382.
[2] SS,沉T,德A,等。X基因GPC3是[J]. , 2000, 19(3): 410-416.
[3] MG、E、L 等人。在 [J] 中的和 -3。和, 2003, 80(2): 221-232.
[4] 陈C, X, Ying Z, et al. -3 可以是 - 吗?[J]. 和, 2017,6(1): 1-6.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话