欢迎光临吉康旅!
根据该研究结果,2018年4月,美国FDA批准奥希替尼用于EGFR突变非小细胞肺癌的一线治疗。通俗的讲,肺癌患者如果携带EGFR突变,不管是否存在,都可以根据自己的情况来使用。选择是否直接用奥希替尼治疗。
2019年8月31日,中国国家药品监督管理局正式批准奥希替尼用于一线治疗EGFR突变晚期非小细胞肺癌。
目前奥希替尼已经被肺癌患者广泛使用,但是随着适用人群的增加,各位癌友不禁担心奥希替尼已经是第三代靶向药,第四代靶向药还没有尚未获准上市。那么奥希替尼一线治疗后出现耐药怎么办?
奥希替尼耐药后基因检测更好
奥希替尼耐药患者使用的治疗方案实际上因人而异。与其盲目采用一种方案,不如先做基因检测。这是因为奥希替尼的耐药机制在个体之间差异很大,而NGS(下一代测序)可以检测到大量未知基因变异,有助于找到奥希替尼耐药的机制,从而对症下药。
一项回顾性研究显示,在奥希替尼耐药后接受NGS基因检测的肺癌患者中位无进展生存期为5.4个月,明显长于未进行NGS检测2.9个月的患者。另一方面,未进行NGS检测的患者在靶向治疗、化疗或最佳支持治疗后,未进行NGS检测的患者客观缓解率明显高于未进行NGS检测的患者(16.2% vs 1< @1.1%)。这表明接受 NGS 检测的患者有更好的治疗结果。
如果您想了解更多关于基因检测的前沿新闻或有需要权威专家解读的基因检测报告,请咨询无癌家庭医疗部。
相关文章:70%的非小细胞肺癌有靶向药物可用,使用基因检测“在靶”有望成为“超长幸存者”!
探寻肺癌原罪——基因检测,你的顾虑都在这里!
奥希替尼的耐药机制在底部,记得对症下药
目前,对奥希替尼治疗的耐药大致可分为四类,包括EGFR通路突变、旁路激活、组织学转化和不明原因的耐药机制。由于有组织学转化的患者,在奥希替尼耐药后,如果条件允许可以做病理检查。
值得注意的是,今年ASCO首次发表了一项研究,证明了基于组织检测的一线和二线奥希替尼耐药机制的比较。一线奥希替尼比二线奥希替尼具有更多未知的耐药机制。在二线耐药后,存在更高的EGFR途径获得性耐药。
一线和二线奥希替尼耐药机制的差异
1 EGFR途径获得性耐药
1 个 C797 位点突变
C797位点突变是最早发现的奥希替尼耐药机制之一。作为不可逆的EGFR-TKI共价结合位点,该位点突变会影响不可逆的EGFR-TKI与相应蛋白区域的结合。对于位点突变介导的耐药,可以尝试单药第一代可逆EGFR-TKI,目前观察到的耐药突变发生率可高达28%。
2 介导耐药性
已经针对介导耐药开展的一些相关临床研究正在探索克服奥希替尼耐药的联合治疗模式,包括I期联合特异性双抗体JNJ-372、联合单克隆抗体和联合HER3抗体等。 ,该研究进一步探讨了奥希替尼联合吉非替尼治疗获得性耐药的可行性。
3 联合耐药突变
对于临床上复杂的耐药突变,临床前研究和相关病例报告显示,()与EGFR单克隆抗体[()或()]联合使用可以有效克服这种耐药性。药物机制。
对于EGFR敏感突变和EGFR联合用药,临床前数据显示奥希替尼联合EGFR变构抑制剂有一定疗效。此外,基于第四代EGFR-TKI BBT-176的I/II期临床研究即将启动。目前,对于耐药后无法进入临床研究的患者,推荐标准化疗。
疾病控制率100%,我国自主研发的广谱新药JMT-101登场!临床招募正在进行中
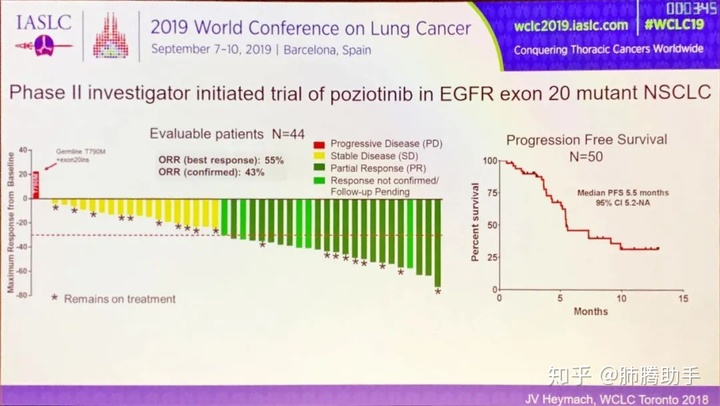
EGFR是肺癌中最常见的突变类型,但在这些突变中,有一个比较少见的突变亚型——EGFR外显子20插入突变,对各种EGFR-TKI药物不敏感,患者治疗难度很大.
令人激动的是,2019年,我国自主研发的专门针对EGFR患者的新药JMT-101获批临床试验!并且在2020年ASCO线上会议上,首次公布了该药在晚期大肠癌患者中的试验结果,疾病控制率达到100%,引起轰动。
好消息是,JMT-101治疗各种实体瘤的I期临床试验已陆续启动。其中,治疗非小细胞肺癌的Ib期试验正在招募患者。如果您想参加临床试验,请咨询无癌家庭医疗部或私信给编辑。
2 获得的 MET 扩增
奥希替尼治疗进展后,MET 扩增耐药占 10% 至 24% 的患者。目前,对MET扩增的评估主要依靠NGS(二次测序)基因检测或FISH检测。研究表明,奥希替尼联合MET抑制剂在EGFR-TKI治疗进展后患者的ORR为30%,中位缓解持续时间为7.9个月。此外,研究中还有相应的MET抑制剂。队列正在进行中。
之前的一些研究也报道了奥希替尼联合克唑替尼治疗获得性MET扩增和MET外显子14跳跃突变的患者的临床可行性和安全性,而国外专家认为,对于不能参加MET抑制剂相关临床试验的患者可以考虑关闭- 使用克唑替尼联合奥希替尼进行标记治疗。
MET/EGFR双特异性抗体JNJ-372在MET扩增患者中也显示出疗效,但能否成为MET/EGFR-TKI联合治疗取得进展后的有效策略,还需等待进一步的临床研究数据。
疾病控制率94.4%!肺癌新药布瑞替尼临床试验招募正在进行中
MET的主要突变类型是MET外显子14跳跃突变,20年前首次发现,但直到最近几年才正式开展针对该靶点的药物研究。
近日,中国药企自主研发的c-MET抑制剂药物布瑞替尼()取得了较为满意的疗效数据。
在最近的 AACR 大会上报告的数据显示,在所有 36 名可评估疗效的患者中,布瑞替尼的客观缓解率(ORR)为 30.6%(11/36),疾病控制率( DCR) 为 94.4% (34/36)。
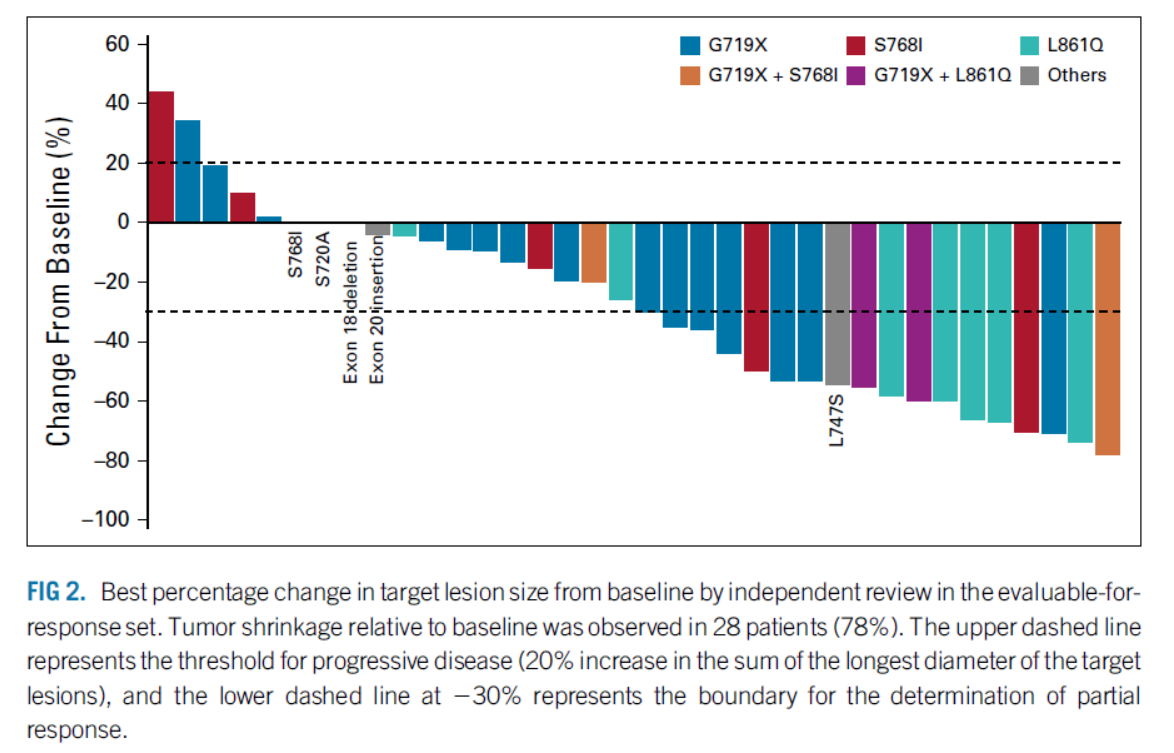
目前,贝瑞替尼II期临床招募正在进行中,国内患者免费使用c-MET靶向药物的机会来了!详情请联系无癌之家。
3 其他旁路激活:融合变体
目前临床观察到的对奥希替尼融合变异体的耐药性包括RET、ALK、BRAF等癌基因。对于这部分耐药机制,基本的治疗策略是结合EGFR抑制剂和融合基因相应抑制剂。
既往回顾性研究报道了联合 BLU-667(RET 抑制剂)、艾乐替尼()或克唑替尼(ALK 抑制剂)、曲美替尼(MEK 抑制剂)来克服融合突变耐药性治疗,然而,在奥希替尼联合曲美替尼的回顾性研究中,毒性非常严重并观察到副作用,提示不同抑制剂的组合应谨慎对待。如需参与临床试验,请咨询无癌家庭医疗部或私信小编。
相关文章:收藏!肺癌临床试验招募信息汇总(7月最新)
在临床实践中需要注意的是,仅基于NGS检测可能无法完全检测出融合突变,同时还应结合RNA融合基因检测。目前,正在对融合基因介导的耐药机制联合治疗模式进行前瞻性探索。
4 组织学转化
一线奥希替尼进展后高达 15% 的患者发生组织学转化,这表明这些临床患者需要进行组织重新活检。与原发性 SCLC 相似,经历小细胞转化的 EGFR 突变具有高频率的 RB1 失活和 TP53 突变以及 EGFR 通路信号传导的丢失。TP53 和 RB1 变体在小细胞转化后不是特定的分子特征,但在基线处汇集 TP53 和/或 RB1 变体显着增加了小细胞转化的概率。对于临床检测到 RB1 和 TP53 突变的患者,需要进一步的组织检测来评估是否存在小细胞转化。
对于小细胞转化患者,推荐EP方案化疗。在一项回顾性研究中,小细胞转化后使用EP方案,54%的患者对治疗有临床反应,中位生存时间为10.9~13.7个月,无随后接受单药免疫治疗的 17 名患者中有 17 名有效。但由于时间敏感的原因,这些患者没有被转诊,研究结果采用了免疫联合化疗。在细胞转化患者中,免疫联合化疗是否可行仍有待相关临床研究进行。
此外,临床实践中也观察到部分鳞癌转化介导的EGFR-TKI耐药,但相关研究报道较少。目前,建议根据组织学选择更合适的化疗方案。今年ASCO报道了一项奥希替尼联合贝伐单抗作为一线治疗的I/II期研究,其中21个进行性病灶进行了组织NGS和病理学评估,EGFR通路获得性耐药突变分别仅为8%、15%病灶有鳞状细胞转化,8%有小细胞转化,61%的患者有未知的耐药机制。然而,本研究的样本量有限,
肺癌靶向治疗的前提——基因检测
现在,我们有很多治疗选择。肿瘤学家可以更精确地选择疗效更好、耐受性更好的疗法,这对患者来说是一个福音。越来越多的肺癌患者将在科学和精准医学的指导下,合理轮换用药。延长生存期,与肿瘤长期生存,将肺癌转为慢性病的梦想已成为现实。
对于肺癌患者来说,早期基因检测是绝对必要的。有助于选择化疗(这将是大多数患者的选择)和靶向治疗。还需要免疫组化研究来了解PD-L1水平等,当然要找到基因靶点,还需要对靶点和TMB进行综合分析。NCCN指南明确建议肺癌患者进行全基因组测序以全面检测突变靶点,而不是EGFR/ALK等个别常见靶点。如何选择基因检测公司,请参考:每个癌症患者都需要做的基因检测,这十个问题一定要搞清楚!
权威专家推荐
王自平
北京大学肿瘤医院
主任医师、研究生导师
胸肿瘤科
赵军
北京大学肿瘤医院
主任医师 副教授
胸肿瘤科
焦顺昌
中国人民解放军总医院肿瘤内科
主任医师、教授
, 医学博士
胸部肿瘤学助理教授
Lowe 胸肿瘤中心临床主任(教授)
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话