欢迎光临吉康旅!
肺癌是癌症死亡的首要原因,占所有癌症死亡的 18.4%。非小细胞肺癌()占所有肺癌的 85%,肺腺癌占所有肺癌的 40%。它们中的大多数是由突变驱动的,并分为不同的分子亚群。最常改变的基因是EGFR(10%-35%)。)、KRAS (25%-30%)、FGR (20%)、ALK (3%-7%)、MET (2%-4%)、BRAF (1%-3%)、ROS1 (1%-3 %) %) 和 RET (1%-3%),部分分子亚组已批准靶向治疗,部分分子亚组正在研究中,如 EGFR 外显子 20 插入突变、外显子 18 改变和 HER2 扩增。本文将重点介绍较为常见的肺癌驱动突变的靶向治疗及其发展方向。
EGFR突变
EGFR信号通路突变在EGFR的发生发展中非常重要,其激酶激活突变或EGFR表达增加导致EGFR通路功能上调,导致突变肿瘤细胞不受控制地增殖。EGFR突变在腺癌、非吸烟者、女性和亚洲人中更为常见。EGFR突变主要发生在酪氨酸激酶结构域外显子18-21,外显子19缺失和外显子21突变占EGFR突变的大部分。识别特定的 EGFR 突变很重要,包括致敏突变、原发性耐药突变、从头和获得性耐药突变。EGFR突变检测是诊断性评价标准,EGFR突变的存在与否极大地影响治疗选择。
研究表明,12%-34% 的 EGFR 突变患者携带非典型或罕见的 EGFR 突变。罕见的EGFR突变是多种多样的,包括各种点突变和外显子18-21插入突变,其中最常见的是外显子20插入突变(9%)和外显子18点突变/A/C(统称为外显子20插入突变) ) G719×,占11.5%)、20外显子(5.5%)、21外显子(5.85%)。一些罕见的突变对酪氨酸激酶抑制剂(TKI)治疗有益,如 G719× 和点突变,但也有罕见的对 TKI 治疗不敏感的 EGFR 突变,如外显子插入突变(约 9% 的 EGFR突变) ) 通常对标准 EGFR TKI 具有抗性,阿法替尼的客观缓解率 (ORR) 为 11%,吉非替尼/厄洛替尼的客观缓解率 (ORR) 为 0%,平均无进展生存期 (PFS) 不到 2 个月。与其他常见突变(ALK、KRAS、常见EGFR突变)驱动的类似,罕见的EGFR突变用免疫检查点抑制剂治疗效果不佳,常见突变驱动患者免疫治疗的中位PFS为2.8 EGFR 外显子 20 插入突变患者的 PFS 为 2.7 个月。因此,有必要识别治疗相关的致癌驱动突变,识别哪些靶向治疗敏感,识别主要耐药机制,发现新的和获得性耐药突变。KRAS,常见 EGFR 突变),罕见 EGFR 突变,免疫检查点抑制剂治疗效果不佳,常见突变驱动患者的免疫治疗中位 PFS 为 2.8 EGFR 外显子 20 插入突变患者的中位 PFS 为 < @2.7 个月。因此,有必要识别治疗相关的致癌驱动突变,识别哪些靶向治疗敏感,识别主要耐药机制,发现新的和获得性耐药突变。KRAS,常见 EGFR 突变),罕见 EGFR 突变,免疫检查点抑制剂治疗效果不佳,常见突变驱动患者的免疫治疗中位 PFS 为 2.8 EGFR 外显子 20 插入突变患者的中位 PFS 为 < @2.7 个月。因此,有必要识别治疗相关的致癌驱动突变,识别哪些靶向治疗敏感,识别主要耐药机制,发现新的和获得性耐药突变。
建议进行生物标志物检测以识别 EGFR 特异性突变以指导靶向治疗。NCCN 指南建议,在确定转移性疾病的组织学亚型后,应在符合条件的患者中进行生物标志物检测。非鳞状细胞应检测 EGFR、ALK、ROS1、KRAS、BRAF、RET、MET 外显子 14 跳跃、NTRK 1/2/3 和 PD-L1。ASCO 还建议任何非鳞状组织、任何具有腺癌成分的组织、临床/人口学特征表明可能存在生物标志物驱动的恶性肿瘤(例如,年龄≤50 岁、从不吸烟或轻度吸烟),都应进行突变检测。对于罕见的 EGFR 突变,通常更推荐使用大型生物标志物面板进行初步筛查。
EGFR突变检测可以使用组织或血液进行,两种方法各有利弊。组织检测非常敏感,新诊断患者的组织很容易获得。理想情况下,应该使用新一代测序的组合,因为它可以检测到罕见的和以前未表征的改变,而单基因检测只能识别常见的 EGFR 突变。缺点是组织样本有时可能不足或缺少肿瘤细胞,而且很多不能反映肿瘤的异质性,完成DNA测序需要2-4周。血液突变检测快速且无创,其主要优点是易于检测常见和罕见的突变。主要缺点是不如组织检测灵敏,
当组织活检标本不足或不可用时,液体活检是快速评估新出现的耐药机制的替代选择。该小组根据液体检测结果确定晚期靶向治疗的指南建议,应首先检测手术(活检)标本,并根据是否存在致癌驱动突变进行适当的标准治疗;如果组织样本不足以进行分子检测,可以进行液体活检的分子分析;首选二代测序组合。如果没有二代测序,其他检测至少应包括EGFR、ALK、ROS1、BRAF,根据结果选择标准治疗;鉴于液体活检的高假阴性率,阴性结果应重复组织活检和分子分析;通过免疫组织化学检测所有组织标本的 PD-L1。
罕见EGFR突变靶向治疗进展
对罕见 EGFR 突变生物学的了解有助于开发针对特定类型突变的靶向疗法。针对 EGFR 点突变(G719× 和 )的第三代 TKI 和外显子 20 插入突变的治疗剂已经上市或正在开发中。针对外显子 18 和 HER2 突变的治疗也在开发中。下文介绍了新的 EGFR 靶向治疗的临床数据。
1. EGFR 点突变
(1)阿法替尼
阿法替尼是 FDA 最初批准的第二代不可逆 ErbB 阻滞剂,用于治疗铂类化疗后进展的 EGFR 外显子 19 缺失或外显子 21 替代突变。2018年1月,适应症扩大至治疗3个非典型EGFR点突变(和/或G719×)转移灶,该适应症的批准主要基于汇总分析结果。32 名患者的突变包括 G719×(S、A、C、D 替代),并且可能与其他点突变共存,阿法替尼 40 mg 或 50 mg/d 治疗,确认的 ORR 为 66% (95% CI) , 47-81),21 例缓解期患者中,52% 缓解期≥12 个月,33% 缓解期≥18 个月。

II 期 LUX-Lung 2 研究和随机 III 期 LUX-Lung 3 和 LUX-Lung 6 研究的事后分析表明,在接受阿法替尼治疗的 EGFR 突变晚期(IIIb-IV 期)肺癌中,12%(75 % 600 例)具有罕见的 EGFR 突变。第 1 组(n=38)罕见 EGFR 突变,包括单点突变或重复突变(,,,,,)或外显子 18-21 的组合变化),第 2 组(n=14)罕见EGFR 突变包括单独的外显子 20 中的新突变或与其他突变组合。第 3 组(n=23) 是外显子 20 中的插入突变。第 1 组的患者对阿法替尼治疗的反应最显着,ORR 为71.1%(23/38 例),中位 PFS 为 10.7 个月,中位总生存期(OS)为 19.4 个月。
随后的一项荟萃分析在各种类型的研究中评估了阿法替尼在总共 693 例罕见 EGFR 突变患者中的临床疗效,发现阿法替尼对主要罕见突变(G719×,,,)和复合 EGFR 突变 TKI-naïve 有效患者有很强的治疗活性。主要罕见突变患者的 ORR 为 60%(n=110),复合突变患者的 ORR 为 77%(n=35),治疗失败时间为 10.@ >8) 个月和 14.7 个月。
(2)奥希替尼
奥希替尼是第三代不可逆 EGFR TKI,FDA 批准用于多种治疗适应症,包括转移性 EGFR 抑制剂治疗后的 EGFR 突变、一线转移性肿瘤治疗、外显子缺失或外显子 21 突变切除后的辅助治疗。ASCO 和安大略省健康指南推荐奥希替尼作为外显子 19 缺失、外显子 21 和外显子 20 突变患者的一线治疗。
I期AURA研究使用免疫组织化学分析评估关键通路和肿瘤标志物,如磷酸化EGFR、磷酸化S6、磷酸化AKT、PD-L1和CD8。AURA 研究表明,奥希替尼可调节关键的 EGFR 信号通路并增加免疫细胞浸润。III期研究纳入了419例EGFR突变一线EGFR TKI治疗后的转移性患者,比较奥希替尼与铂类培美曲塞化疗,奥希替尼显着提高中位PFS,从化疗4.4个月到10.1奥希替尼一个月(风险比 [HR],0.30,P<0.001),ORR 太 奥希替尼组更好(71% vs 31%,P<0. @>001). 重要的是,奥希替尼显着改善了 CNS 转移患者的中位 PFS,
奥希替尼组的次要终点中位 OS 为 38.6 个月(95% CI,34.@)。>5-41.8),标准 TKI 组 31.8 个月(95% CI,26.6-36.0)@ > (死亡 HR 0.80, 95% CI 0.64-1.00, P=0.046).12、24 和奥希替尼组 36 个月的 OS 率和继续接受一线研究治疗的患者数量较高,奥希替尼组 ≥3 级不良事件较低(42% 和 47%)。24 和 36 个月的 OS 率和继续接受一线研究治疗的患者数量在奥希替尼组中更高。奥希替尼组的≥3 级不良事件发生率较低(42% 和 47%)。24 和 36 个月的 OS 率和继续接受一线研究治疗的患者数量在奥希替尼组中更高。奥希替尼组的≥3 级不良事件发生率较低(42% 和 47%)。
奥希替尼目前正在评估治疗罕见的 EGFR 点突变,基于对多个 EGFR 突变患者的疗效。一项 II 期研究包括 36 例罕见 EGFR 突变复发和转移的患者,包括 G719×(n=19), (n=9) 和 (n=8), )) ORR治疗后分别为53%、78%和38%,PFS分别为8.2、15.2和12.3个月。
2. 外显子 20 插入突变
EGFR外显子20插入突变是第二常见的EGFR突变,占所有EGFR突变的10%-12%,对第一代、第二代和第三代EGFR TKI耐药主要是由于外显子20插入突变诱导的药物-结合口袋空间位阻。然而,研究表明,具有拉伸的小喹唑啉衍生物(如阿法替尼)可能能够抑制外显子20插入突变,因为它们可以适应空间位阻结合口袋,而不是具有拉伸的大药物基团,如厄洛替尼无法达到残基 C797 并且不能抑制外显子 20 插入突变。
与其他EGFR突变相比,外显子20插入突变预后较差,现有TKI靶向治疗的疗效远不及经典EGFR突变。一项II期研究评估了第三代EGFR TKI奥希替尼/d治疗21例外显子20插入突变患者的疗效,结果显示奥希替尼具有一定的活性,ORR为25%,中位PFS为9.7 个月(95% CI,4.07-NA)。与外显子 19 和 21 的经典 EGFR 突变相比,外显子 20 突变的患者可能从免疫检查点抑制剂治疗中获益更多,但仍然有限(中位 PFS ~2 个月),且治疗相关不良事件的风险较高。
尽管已经评估了外显子 20 插入突变的多种治疗方法,但目前的护理标准是铂类化学疗法。对突变生物学认识的提高促进了针对外显子 20 插入突变的靶向治疗的发展,首个针对外显子 20 插入突变的靶向药物已获批用于二线治疗。
(1)
它是一种完全人源化的双特异性 IgG1 抗体,靶向 EGFR 和 cMET 受体。它是一种具有免疫细胞导向活性的 EGFR 靶向治疗,对 EGFR 突变驱动的肿瘤(包括 TKI 耐药肿瘤)具有显着的临床益处。. 通过 Fc 依赖性单核细胞/巨噬细胞介导的抗肿瘤机制(吞噬作用导致肿瘤细胞受体降解)作用于激活和抗性 EGFR 和 cMET 突变和扩增。
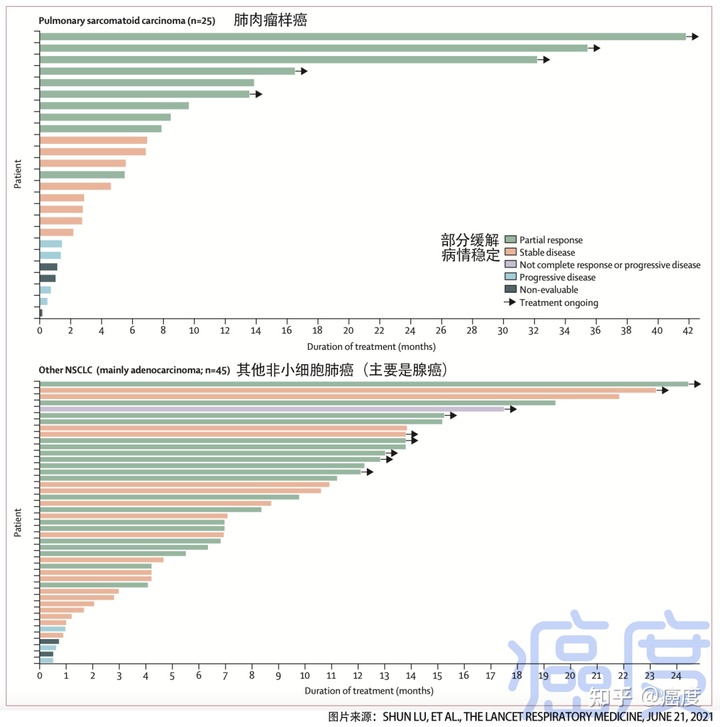
单一疗法对多种 EGFR 突变具有抗肿瘤活性,包括外显子缺失和突变、外显子 20 插入和 MET 扩增。一项 I 期研究报告称,30%(32/108) 患有 EGFR 突变,包括外显子 20 插入突变和 cMET 扩增的患者)在治疗后实现了部分缓解。正在进行的 I/II 期 II 期研究正在评估剂量递增部分单药治疗的推荐 II 期剂量 (RP2D),用于治疗在含铂化疗中取得进展的转移性/不可切除的外显子 20 插入突变患者,
该研究纳入了81名患者,从最初诊断到开始研究的中位时间为17个月,接受过含铂双药化疗,其中25%接受过EGFR TKI治疗,中位年龄为62岁,59%为女性,主要是子群。美国人 (49%) 或白人 (37%)。这项初步研究显示在这组患者中的疗效,根据盲法独立审查确定,ORR 为 40%(95% CI,29-51),中位反应持续时间 11.1 个月) (95% CI,6.9-未达到)临床受益率为 74%(95% CI,63-83),定义为完全缓解,至少 2 次疾病评估部分缓解)或病情稳定。通过下一代测序在 63 名可评估患者中鉴定出 25 种不同的外显子 20 插入突变,所有这些都显示出治疗活性。
(2)
(TAK-788) 是一种具有选择性临床前活性的口服选择性 EGFR/HER2 TKI,可抑制激活的 EGFR 和 HER2 突变,包括外显子 20 插入突变,但不包括野生型 EGFR。28 项 I/II 期研究ECOG PS 0-1 和每日剂量递增治疗对标准治疗无效的晚期疾病患者证实 ORR 为 43%。目标病灶的中位最佳变化为 -32.6% (-100 %~26.3%),中位 PFS 为 7.3 个月(95% CI,4.4-15.@ >6)。
正在一项 3 部分、开放标签、多中心研究(I 期剂量递增、II 期剂量扩展、扩展队列)中评估疗效,其中约三分之二的患者是亚洲和女性,铂类预处理患者 (PPP)队列 先前全身性抗癌方案的中位数为 2,队列为 1。ORR 为 26%(95% CI,19-35) 和 23%(95% CI,15-33))对于 PPP 队列和队列,中位反应持续时间分别为 17.5 个月(95% CI,8.3-不可评估)且不可评估。在数据截止时,超过 50两组中仍有 % 的患者处于缓解期,两组的中位 PFS 为 7.3 个月(95% CI,5.5-10.2)。其他结果还显示出具有临床意义的益处,两个队列中 82%(94/114) 和 80%(77/96) 患者的目标病变直径从基线减小。≥30% 患者的治疗相关不良事件是腹泻) (90%,PPP 和队列 ≥3(分别为 21% 和 16%),皮疹(45%),甲沟炎(35%),食欲下降(0-30%),恶心(0-30%)和干燥皮肤 (30%)。
(3)
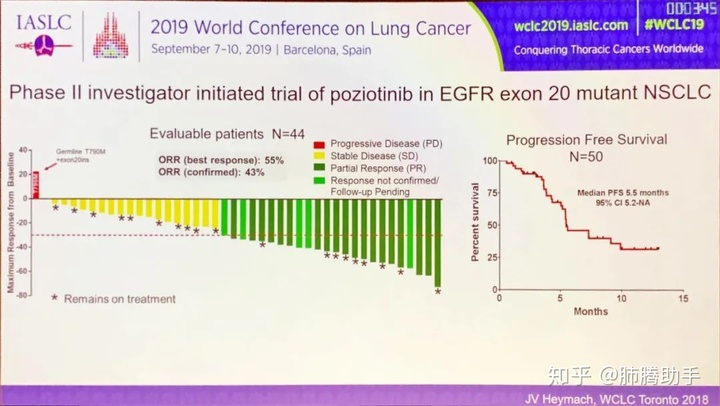
它是一种新型 EGFR TKI 抑制剂,比第一代和第二代 TKI 更小且更具拉伸性,使其能够与由外显子 20 中的插入突变引起的空间位阻药物结合袋结合。外显子 20 插入突变,治疗小鼠的肿瘤体积减少了 80%,而接受阿法替尼治疗的小鼠肿瘤体积增加了 35%。在一项针对 44 名 EGFR 外显子 20 突变患者的 II 期研究中,治疗的最佳 ORR 率为 55%,经证实的 ORR 率为 43%。
一项 II 期研究 ( ) 评估了 115 名 EGFR 外显子 20 插入突变的非初治患者口服(16mg/d)治疗的安全性和有效性,中位年龄为 61 岁,先前治疗线的中位数为 2 , 可评估患者的 ORR 为 19.3% (95% CI, 11.7-29.1), 中位缓解持续时间7.4 个月(95% CI,3.7-9.7),中位 PFS 为 4.1 个月(95% CI,3.7-5. 5). 最常见的≥3 级治疗相关事件是皮疹 (28%)、腹泻 (26%)、口腔炎 (9%) 和甲沟炎 (6%)。
3.不良事件管理
新的靶向治疗不仅对罕见的EGFR突变有治疗效果,而且毒性可控。最常见的≥3级药物相关不良事件是腹泻和皮疹。在这些新药的临床研究中,20%的患者因不良事件而停止治疗,其中许多可以通过减少剂量来控制。
与 EGFR TKI 靶向治疗(阿法替尼、奥希替尼)相关的皮疹管理包括局部润肤剂、局部皮质类固醇和早期皮肤科就诊。用止泻药(如洛哌丁胺、硫酸阿托品)和水合作用早期积极治疗腹泻是有益的。此外,建议监测血清电解质(钾、钠)、肾功能(血清肌酐)和肝功能。减少剂量可降低治疗相关不良事件的风险,尤其是阿法替尼。
EGFR 抗体最常见的不良事件是输液相关反应,以呼吸困难、潮红、寒战和恶心为特征。发生在 65% 的患者中,仅 2% 的患者出现 3 级反应,大多数 (94%) 输液相关反应发生在第 1 周期的第 1 天,中位发病时间为 44 分钟,1% 的患者发生第 2 天 在每个周期的第 1 天,可以通过停止输注并以较低速率重新开始输注来减轻输注相关反应。使用激素、止痛药和/或抗组胺药可以降低输液相关反应的风险和严重程度。
EGFR靶向治疗的未来方向
外显子 20 插入突变和外显子 18-21 点突变是研究最多的,其他几个不太常见的 EGFR 和 EGFR/ERBB 突变也需要研究以进行有效的靶向治疗。研究目前正在评估外显子 18 突变和 HER2 突变和扩增的治疗方法。在主要的罕见EGFR突变中,外显子18突变占5%。有限的临床证据表明 EGFR TKI 阿法替尼和奥希替尼对外显子 18 突变具有一定的治疗活性。/HER2 基因(ERBB/EGFR 家族的另一个成员)中的突变最常发生在激酶结构域的外显子 18-21 中。对 HER2 靶向 TKI 和单克隆抗体的反应因癌症类型和突变而异。在非鳞状细胞癌患者中,约 2.3% 的患者有 HER2 突变,另外还有一个 1.
1.外显子 18 突变
在一项体外研究中,与第一代 TKI 相比,EGFR 外显子 18 突变对(不可逆的 TKI)高度敏感。II 期篮子研究评估 /d 单一疗法的疗效,治疗前 8 周强制口服洛哌丁胺预防,最初 11 名可评估患者的中位年龄 67 岁,55% 男性,91% 白人,55% ECOG PS 1,先前治疗的中位数系为2,大多数患者具有复杂的G719×突变。部分缓解6例,稳定4例,进展1例。单个和复杂的 G719× 突变均对治疗有反应,确认的 ORR 为 40%,反应持续时间 7.5 个月,中位 PFS 为 9.1 个月。没有关于 3 级腹泻的报告。该研究继续招募具有 EGFR 外显子 18 突变的患者。
2.HER2突变
虽然 HER2 突变和扩增在乳腺癌和胃癌中很常见,但在 . 虽然许多针对 HER2 的药物已被批准用于其他类型的癌症,但它们尚未获得批准,研究正在评估这些药物。
Ado- 是一种靶向 HER2 的抗体药物偶联物,最初用于治疗 HER2 转移性乳腺癌。一项 II 期研究评估了 Ado-(3.6mg/kg,每 21 天一次)治疗 18 名 HER2 突变肺癌患者(中位年龄 64 岁)的疗效2 的治疗中,50% 接受了 HER2 靶向治疗。中位随访 10 个月,ORR 为 44%,中位 PFS 为 5 个月。一名病情稳定的患者的 PFS 超过 11 个月,肿瘤缩小 27%。不良事件包括输液反应、血小板减少、肝酶升高、疲劳和恶心,为 1 级或 2 级。本研究结果为阳性。
在一项对 11 名接受抗体-药物偶联物治疗的 HER2 突变患者的 I 期研究中,证明 ORR 为 72.7%。II 期 - 该研究正在评估(6.4mg/kg 每 3 周)治疗 HER2 过度表达或 HER2 激活的非鳞状细胞癌。来自 42 名主要具有 HER2 激酶结构域 (90.5%) 突变的患者的早期结果(中位年龄 63 岁,之前的中位治疗线2) 证实 ORR 为 61.9% , 疾病控制率 90.5%。估计中位 PFS 为 14 个月,中位 OS 尚未达到。所有患者均发生与治疗相关的不良事件(≥ 3 级为 64.3 %) ,导致 59.5% 的患者停药,38.1% 的患者减量,23.8% 的患者停药。
除了靶向 HER2 治疗外,临床研究正在评估其他靶向 EGFR 的 TKI 对 HER2 突变患者的疗效。在一项 II 期研究中,HER2 外显子 20 插入突变患者的口服 16 mg/d 治疗在前 12 名可评估患者中的 ORR 为 42%,中位 PFS 为 5.6 个月。多国 II 期研究包括一组具有 HER2 外显子 20 插入突变的患者(-2,n=90),中位年龄 60 岁,64% 女性,66% 不吸烟者,中位先前治疗线) 16 mg/d 的口服治疗在 74 名可评估患者(90 名患者中的 27.8%)中显示 ORR 为 35.1%,中位 PFS 为 5.5 个月。74%(67/90)患者肿瘤缩小,中位肿瘤缩小22%。达到预期疗效,
参考
JK, JV, B. 现场:在与 EGFR .J Natl Canc Netw 中。2021;19():S1-S11. doi:10.6004/.2021.@ >0200.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话