欢迎光临吉康旅!
酪氨酸激酶抑制剂(TKIs)是治疗非小细胞肺癌(non-cell lung )常用的靶向药物。第三代EGFR-TK1奥希替尼()是EGFR敏感突变和突变患者的标准一线治疗,美国NCCN指南推荐作为首选一线治疗;第三代 ALK-TKI 劳拉替尼()已在美国、日本等国家获批用于接受克唑替尼()或至少一种(如艾乐替尼)或色瑞替尼治疗后出现晚期 ALK 阳性疾病进展的患者()]。不幸的是,所有接受 TKI 治疗的患者都不可避免地会产生获得性耐药。我们来谈谈如果奥希替尼耐药怎么办?呼吸与危重症医学科王志刚,
如何应对第三代EGFR-TKis奥希替尼耐药?
第一种是ECFR依赖的第三代EGFR-TKI耐药后,即我们临床目前使用的奥希替尼耐药后,根据耐药模式准确分层至关重要。
奥希替尼耐药模式分为局部进展、缓慢进展和全身或暴发性进展。其中,局部进展最为常见。对于局部进展和进展缓慢的患者,建议继续奥希替尼治疗或联合放疗、手术等局部治疗,或联合抗血管生成靶向药物。这些患者仍然可以从奥希替尼治疗中受益。50%以上进展缓慢的患者中位无进展生存期可延长3-5个月,局部进展患者中位用药时间可延长4-8个月。当然,这些患者必须密切随访,及时检测驱动基因,以免失去换药机会。
对于暴发性进展的患者,首先要明确突变与ECFR突变的关系。如果是顺式突变,患者对一、二、三代EGFR-TKI耐药,目前还缺乏成熟的治疗方案。. 第二代ALK-TKI布加替尼()可竞争性结合EGFR激酶结构域的ATP结合位点,不受空间位阻影响,因此可抑制(或)++顺式三突变肿瘤790M+顺式突变对布加替尼联合西妥昔单抗的治疗也有效;由于此时肿瘤细胞对ECFR信号通路的依赖程度较低,因此它们对VEGF更敏感。因此,奥希替尼联合贝伐单抗可继续治疗,可达到理想的效果(PFS可达9个月);如果+是反式突变,第一代EGFR-TKI联合第三代EGFR TKI仍然敏感,布加替尼联合西妥昔单抗、化疗和免疫检查点抑制剂都是可选方案;第一代EGFR-TKI可用于单突变。单独或联合使用 EGFR 单克隆抗体(如帕尼单抗、西妥昔单抗)是克服 EGFR 突变的潜在策略;动物实验表明,西妥昔单抗联合EGFR变构抑制剂在存在EGFR+和EGFR突变的情况下有效。+ + 突变具有明显的治疗作用,其主要机制与部分抑制EGFR + 和突变细胞中的EGFR 活化有关。布加替尼联合西妥昔单抗、化疗和免疫检查点抑制剂都是可选方案;第一代EGFR-TKI可用于单突变。单独或联合使用 EGFR 单克隆抗体(如帕尼单抗、西妥昔单抗)是克服 EGFR 突变的潜在策略;动物实验表明,西妥昔单抗联合EGFR变构抑制剂在存在EGFR+和EGFR突变的情况下有效。+ + 突变具有明显的治疗作用,其主要机制与部分抑制EGFR + 和突变细胞中的EGFR 活化有关。布加替尼联合西妥昔单抗、化疗和免疫检查点抑制剂都是可选方案;第一代EGFR-TKI可用于单突变。单独或联合使用 EGFR 单克隆抗体(如帕尼单抗、西妥昔单抗)是克服 EGFR 突变的潜在策略;动物实验表明,西妥昔单抗联合EGFR变构抑制剂在存在EGFR+和EGFR突变的情况下有效。+ + 突变具有明显的治疗作用,其主要机制与部分抑制EGFR + 和突变细胞中的EGFR 活化有关。西妥昔单抗)单独或联合使用是克服 EGFR 突变的潜在策略;动物实验表明,西妥昔单抗联合EGFR变构抑制剂在存在EGFR+和EGFR突变的情况下有效。+ + 突变具有明显的治疗作用,其主要机制与部分抑制EGFR + 和突变细胞中的EGFR 活化有关。西妥昔单抗)单独或联合使用是克服 EGFR 突变的潜在策略;动物实验表明,西妥昔单抗联合EGFR变构抑制剂在存在EGFR+和EGFR突变的情况下有效。+ + 突变具有明显的治疗作用,其主要机制与部分抑制EGFR + 和突变细胞中的EGFR 活化有关。
和 2 种尚未上市的新型第四代药物,它们是突变 EGFR 的变构非 ATP 竞争性抑制剂。EGFR -1 ( )因其对突变EGFR的高度选择性而备受关注,但对EGFR的进一步研究表明其对+突变体的作用有限。该化合物经过优化,对 EGFR+ 突变具有活性,对野生型 EGFR 具有高度选择性。然而,仅部分抑制细胞中的 EGFR 磷酸化,并且在具有 + 突变的细胞中显示出较弱的抗增殖活性。与西妥昔单抗联用可防止 EGFR 二聚化并在 EGFR+ 突变 Ba/F3 细胞和小鼠异种移植模型中引发显着的抗肿瘤增殖反应,在三级突变细胞系协同效应中也观察到相同的情况。与西妥昔单抗共同给药导致 ++ 突变模型中显着的肿瘤缩小。临床疗效需要通过临床试验来验证。
第二种情况,不依赖EFGR的第三代耐药怎么办?
联合治疗是延缓奥希替尼耐药的有效措施。MET抑制剂克唑替尼的组合或单独使用可以延迟或逆转MET扩增诱导的奥希替尼耐药。2019年4月,在美国癌症研究协会(AACR)年会上,有报道称国产新药沃利替尼()对外显子跳跃有很好的抑制作用(ORR 54.8%),而胃肠道非替尼联合()、吉非替尼联合萨沃利替尼、奥希替尼联合萨沃利替尼、奥希替尼联合克唑替尼、奥希替尼联合卡博替尼可作为MET基因异常导致奥希替尼耐药的替代策略;联合或单用HER-2抑制剂曲妥珠单抗可延缓HER-2基因扩增引起的奥希替尼耐药,奥希替尼与TDM-1或奥希替尼联合拉帕替尼可能对HER-2扩增引起的奥希替尼耐药有效;K-RAS突变引起的奥希替尼耐药可选用奥希替尼联合司美替尼/曲美替尼;曲美替尼抑制MEK1/2的活性,从而抑制BRAF突变引起的奥希替尼耐药;联合可强烈抑制由P13K抑制剂、SFK抑制剂、FAK抑制剂、AXL抑制剂等引起的BRAF突变奥希替尼耐药,可延缓奥希替尼耐药。PTEN 突变和突变诱导的奥希替尼耐药可能通过使用 mTOR 抑制剂依维莫司有效,它是 PI3K/AKT 通路的下游丝氨酸苏氨酸激酶。对于RET重排引起的奥希替尼耐药,
需要强调的是,化疗仍然是非小细胞肺癌患者的主要治疗手段之一。对奥希替尼耐药患者的化疗方案选择可基于驱动基因阴性的晚期非鳞状细胞癌和鳞状细胞癌。对于替尼耐药的患者,PD-1/PDL-1抑制剂可能有一定的疗效。
特别要提醒的是,对于那些没有获批靶向药物的脱靶突变,建议参加国家批准的合法临床试验。
相关链接:据报道,JNJ-372、U3-1402、,四种新药,解决奥希替尼耐药和难治性突变。
(1)JNJ-372:同时阻断EGFR和MET,后线治疗ORR为30%,对各类耐药突变均有效。
JNJ-372(JNJ-)是强生公司和丹麦公司基于该平台开发的靶向EGFR和cMet的人源化双特异性抗体。JNJ-372能同时抑制EGFR和cMet的磷酸化,以及下游信号的激活,具有很强的ADCC(抗体依赖性细胞介导的细胞毒性)。2019 年 ASCO 大会展示了其调查结果。1 期研究招募了 108 名先前接受过 JNJ-372 治疗的晚期 EGFR 突变(包括敏感突变和其他罕见突变)患者。结果,后线治疗的 ORR 高达 30%,疗效分布在各种 EGFR 亚型中。这些患者包括突变、MET 扩增和先前对奥希替尼的耐药性。此外,JNJ-372对ins也有影响。在亚组分析中,DCR(疾病控制率)居然达到了100%!ORR(客观缓解率)为 30%(其中 2 例为 耐药患者)。这样的数据给难治性患者带来了新的希望。通过双靶点抑制,JNJ-372对继发于EGFR-TKI耐药的多种突变类型(包括MET和)具有疗效,耐受性良好(3级及以上不良反应发生率仅为9%),有望成为未来克服EGFR耐药的新星。
(2)U3-1402:抑制HER3解决耐药性,颅内控制率可高达85.7%。
在 57%-67% 的 EGFR 突变患者中发现了不同水平的 HER3 ( ) 表达。对此,公司研发了一种名为U3-1402的新型ADC(抗体偶联药物),它利用全人源化HER3抗体与新型拓扑异构酶1抑制剂通过四肽接头连接,使抗体上附着更多的细胞毒素,可能具有更强的肿瘤杀伤作用。2019年ASCO大会上,一款代号为U3-1402的新药诞生了。初步数据显示,它可以全面对抗各类EGFR-TKI治疗耐药,甚至奥希替尼耐药也有希望。在刚刚结束的世界肺癌大会(WCLC)上,U3-1402的更新数据发布,再次显示了这款新药解决奥希替尼耐药问题的希望。更新数据显示,30例EGFR突变晚期非小细胞肺癌()患者在I期临床试验中,包括17例EGFR患者、12例EGFR患者、1例患者之前接受过EGFR TKI治疗,且15例患者曾接受过化疗,28例也使用过奥希替尼。所有患者均为IV期,其中脑转移15例(50%),肿瘤组织中HER3表达25例,阳性率为100%。U3-1402疾病控制率接近100%。在 23 名可评估患者中,22 名肿瘤缩小,疾病控制率大于 95% DCR。17例仍在治疗中。U3-1402对EGFR-TKI不同耐药机制的患者有效,如常见,HER2和CDK4扩增可以控制。22例患者(包括2例//,5例Del 19//)观察到肿瘤缩小,6例患者达到PR(包括3例Del 19//),ORR为26%。14例可评价的脑转移患者中,ORR为28.6%,DCR为85.7%,死亡1例,仍在治疗中5例,其中3例已治疗6%以上个月。
(3)TAK-788用于治疗难治性20个插入突变,已开展III期临床研究。
另一个问题是可治疗的 TAK-788。该药物已进入 III 期临床研究 (),将晚期患者与化疗作为一线治疗进行比较。而TAK-788也在国内二期二线临床试验中。数据显示,TAK-788治疗的ORR可达43%,DCR为86%,中位PFS(无进展生存期)为7.3个月。
(4)国产IV代。
以往研究的结果可以解决耐药性的爆发。
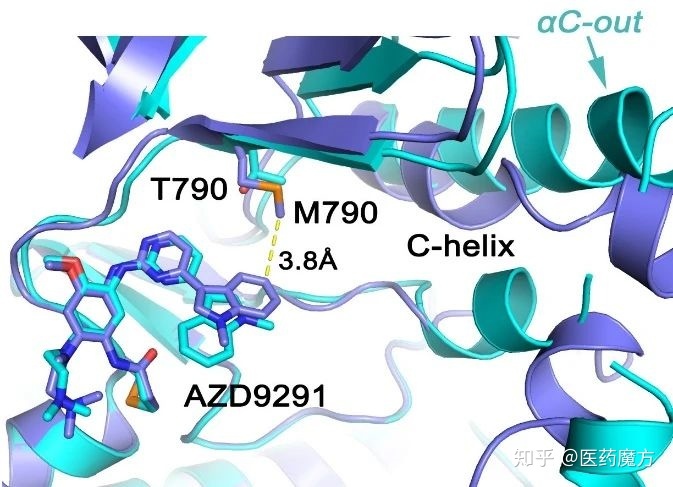
奥希替尼在对后期治疗产生耐药性后有 21% 的机会发生继发性突变。该突变是半胱氨酸残基向丝氨酸的错义突变,破坏了EGFR蛋白与第三代靶向药物的结合,从而未能阻止EGFR蛋白与ATP的结合以及下游信号通路的激活. 目前对于奥希替尼耐药后易发生的两个三重突变://和//这两种突变的反应,目前还没有成熟的标准,临床需求迫在眉睫。
在2019年AACR大会上,我国正大天庆药业集团研发的第四代口服EGFR靶向药物的初步实验结果公布,为解决奥希替尼耐药带来了希望。除了解决奥希替尼耐药外,该药还对1/2代TKI耐药后的双突变有效。研究表明,d746-750()//, //, d746-750/ and/的IC50(杀死一半癌细胞所需的药物浓度)为0.46,0.13、0.26、0.19nM,提示它们对1/2/3代TKI耐药后EGFR三双突变的肿瘤细胞具有良好的抑制能力。相比之下,奥希替尼的抑制能力较弱。在不同型号的 //, 它可以很好地延缓肿瘤的生长,但奥希替尼不能阻止肿瘤的生长。一期研究()计划招募30名受试者,口服给药28天,每天一次,主要研究者为吴一龙教授,地点为广东省人民医院。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话