欢迎光临吉康旅!
肿瘤分子靶向药物临床应用进展引言自1997年第一个分子靶向药物利妥昔单抗()获批用于治疗CD20阳性B细胞淋巴瘤并取得满意的治疗效果以来,一直是新型抗肿瘤药物分子靶点不断涌现。2000年至2009年3月,美国FDA共批准了19个此类新药,而同期美国批准的传统化疗新药仅有8个。目前FDA注册的临床试验有1个,其中其中1506个现代医学肿瘤治疗的重要里程碑与肿瘤分子靶向治疗有关。, 拓扑异构酶抑制剂靶向治疗, 个体化诊疗总结一、靶向治疗药物概述二、 靶向药物分类及代表性药物介绍三、分子靶向药物面临的问题一、靶向治疗药物概述什么是靶向治疗?在细胞和分子水平上,利用确定的致癌位点(该位点可以是肿瘤细胞内的蛋白质分子或基因片段)来设计相应的治疗药物。药物进入体内后,特异性选择这些致癌位点结合作用,在不影响肿瘤周围正常组织细胞的情况下,使肿瘤细胞特异性死亡,因此分子靶向治疗又被称为“生物导弹”。药物靶向治疗的效果取决于靶向药物的特性以及肿瘤内是否存在靶向药物的分子靶点及其异常状态。
抗肿瘤药物作用机制不同 传统化疗的缺点 对肿瘤细胞的非特异性杀伤 对肿瘤细胞有抵抗力 对某些类型肿瘤的疗效改善不大 疗效较高 2. 对肿瘤相关分子靶点的特异性作用 34. 杀伤作用对耐药细胞 靶向药物和化疗药物的协同作用杀死缺乏特异性靶点的肿瘤具有化疗的非选择性杀伤作用 对化疗药物不敏感或耐药的细胞杀伤细胞去除最小的残留病灶。理想的靶向抗肿瘤药物以高特异性与靶分子结合。当与目标分子结合时,它们具有高亲和力和小分子量。组织中渗透性和稳定性的分子化学结构有利于延长药物在体内的半衰期。与治疗对象生物学同源,最大程度避免宿主异种蛋白反应。肿瘤治疗的新靶点是恶性表型的新靶点。非常重要的大分子 1 理想的肿瘤靶点 在重要器官和组织中无显着表达 2 生物学相关性 3 在临床标本中可重复检测 4 与临床结果显着相关 5 目前上市的FDA批准的靶向药物 抗肿瘤靶向药物处于后期开发阶段美国二、靶向药物分类及代表性药物介绍(一)
此后,单克隆抗体在抗肿瘤、类风湿关节炎和自身免疫系统缺陷领域得到大力推广。由于具有选择性杀伤癌细胞的能力,具有高效、低毒的特点,在肿瘤治疗中发挥着越来越重要的作用。近20年来,FDA批准了近20个单克隆抗体药物,其中9个药物用于肿瘤治疗。FDA批准的抗肿瘤单克隆抗体商品名目标抗体类型适应症阿仑单抗CD52人源化非结合慢性粒细胞白血病贝伐单抗人源化非结合结直肠癌非鳞状和乳腺癌西妥昔单抗EGFR嵌合非结合结直肠癌,头颈部肿瘤 CD33 人源化卡霉素偶联物 急性髓细胞白血病 钇 90- CD20 鼠,钇 90 偶联物 非霍奇金淋巴瘤 帕尼单抗 EGFR 人,非偶联物 结直肠癌 利妥昔单抗 CD20 嵌合,非偶联物 非霍奇金淋巴瘤,类风湿性关节炎 碘131- CD20 , 131 Non-'s HER-2 2. 非偶联 HER-2 过表达的乳腺癌单克隆抗体的组成人,并且在输注过程中存在过敏反应的风险。此外,接受此类单克隆抗体治疗的患者通常会产生抗小鼠蛋白抗体,
近年来开发的单克隆抗体已经含有或含有较高比例的人体成分蛋白,其中嵌合抗体含65%,人源化抗体含95%,人源抗体含100%人体蛋白。抗体的类型也可以从其药名的后缀来识别,即~(-)是鼠类的,~(-)是嵌合的,~(-)是人的。α和α-β单克隆抗体(-)是人型单克隆抗体。单克隆抗体结构 单克隆抗体分类 抗肿瘤单克隆抗体分为两大类:1)抗肿瘤单克隆抗体药物,可以与肿瘤细胞结合,通过直接的抗原抗体反应引起细胞死亡,如抗-肿瘤单克隆抗体。CD20嵌合抗体利妥昔单抗(),抗血管内皮生长因子(VEGF)贝伐单抗()等;2)抗肿瘤单克隆抗体偶联物,以单克隆抗体为载体,与放射性核素、免疫毒素或细胞毒素偶联形成单克隆抗体偶联物,通过单克隆抗体与肿瘤细胞结合,利用放射性核素、免疫毒素或细胞毒素杀伤细胞,如抗CD20抗体和131I偶联托西木单抗(商品名:)、抗CD33重组人源化单克隆抗体和抗生素加利车霉素()偶联物等。单克隆抗体的结构特点是体积小,穿透性好,能更有效地渗透到肿瘤中;分子小、消除快、半衰期短、累积毒性低;他们携带的弹头分离后,可以快速清理;循环中的免疫系统 靶向结合物对靶细胞几乎没有竞争;它们可以穿过血脑屏障,因此使用单克隆抗体偶联物可以更好地达到治疗目的。
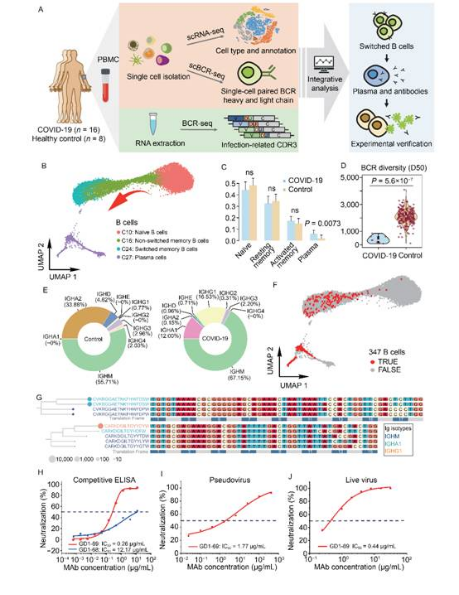
单克隆抗体治疗肿瘤1)与靶细胞特异性结合的生物学基础:免疫电镜和放射性同位素检测表明抗体药物对肿瘤靶细胞具有特异性结合和内化作用。----治疗基础2)选择性杀伤靶细胞:体外试验,显示选择性杀伤肿瘤靶细胞。---- 治疗依据。3)具体分布:放射自显影显示药物高度集中在活肿瘤细胞区域,并在肿瘤内部血管附近局部分布。----靶向治疗4)提高疗效,降低毒性:抗体偶联物和非偶联抗体均可在体内表现出抗肿瘤作用。动物实验结果也表明,各种偶联物都不同程度地增强了药效,降低了毒性。----协同减毒单克隆抗体的抗肿瘤机制 单克隆抗体药物的合理应用原则1)孕妇及哺乳期妇女、严重骨髓抑制、过敏体质或敏感体质者禁用。2)在一些患者中反复给药导致免疫球蛋白水平显着下降,甚至并发肺部感染。3)肺病、充血性心力衰竭、肝肾功能不全、高血压、心脏病患者慎用。4)注意单克隆抗体综合征。单克隆抗体药物合理应用原则5) 单克隆抗体的首次输注反应发生率较高。为预防严重的过敏反应,可在给药前口服苯海拉明和对乙酰氨基酚。6)一旦发生过敏性休克,立即给予肾上腺素、皮质类固醇、苯海拉明、支气管扩张剂和氧气。7)蛋白质结构在胃肠道中变性,必须静脉内给药。
8)单克隆抗体不被肝脏代谢,所以没有明显的药物相互作用。实体瘤单克隆抗体治疗存在的问题1)嵌合单克隆抗体进入人体后可能引起物种排斥,导致产生人抗鼠抗体(HAMA),引起严重过敏反应等不良反应< @2)实体瘤细胞被致密的基质包围,单克隆抗体很难穿透这道屏障;3)单克隆抗体的生产成本和价格非常昂贵;4)肿瘤细胞由于异质性,含有某种受体的肿瘤细胞的单一消除并不代表肿瘤的治愈。代表性药物利妥昔单抗(,)——抗CD20单克隆抗体,可特异性结合鼠可变区人κ恒定区人IgG1的CD20 Fc片段 1997年11月 它是第一个用于临床的肿瘤靶向治疗药物。它特异性结合CD20抗原并诱导抗体依赖性细胞介导的细胞毒性(ADCC)和补体介导的细胞溶解作用以杀死靶细胞,从而杀死靶细胞。抑制B细胞增殖,诱导B细胞凋亡,提高肿瘤细胞对化疗的敏感性。临床适应症 治疗复发性或耐药性滤泡性中央淋巴瘤(国际工作班 B、C 和 D 亚型的 B 细胞非霍奇金淋巴瘤)。CD20 阳性弥漫性大 B 细胞非霍奇金淋巴瘤 (NHL) 应与标准 CHOP 化疗(环磷酰胺、多柔比星、
用法用量 成人单药,推荐剂量为/m2,静脉给药,每周一次,共4次。止痛药(如对乙酰氨基酚)和抗过敏药(如盐酸苯海拉明)可在输注该药前 60 分钟服用。初始输注:推荐的初始输注速率为 50 mg/h;前 60 分钟后,可每 30 分钟增加 50 mg/h,直至达到最大速率/h。后续滴注:利妥昔单抗滴注可以以 /h 的速率开始,每 30 分钟 /h 增加一次,最大速率为 /h。如果发生过敏或输注相关反应,应暂时减慢或停止输注。如果患者的症状有所改善,输入速度可以提高一半。用药注意事项 利妥昔单抗的最佳输注浓度为 1 mg/ml。利妥昔单抗不应该未经稀释作为静脉滴注给药,也不能将准备好的注射液用作静脉推注。利妥昔单抗治疗后最常见的不良反应是输注相关反应,治疗前静脉注射糖皮质激素显着降低了这些事件的发生率和严重程度。镇痛药和抗组胺药应在开始输注利妥昔单抗前 30 至 60 分钟预先给药。如果使用的方案不包括皮质类固醇,也应预先给予糖皮质激素。曲妥珠单抗(赫赛汀)——抗 HER-2 单克隆抗体于 1998 年 9 月 25 日上市。它是人 IgG1 稳定区和小鼠来源的抗 HER-2 胞外区单克隆抗体的组合。
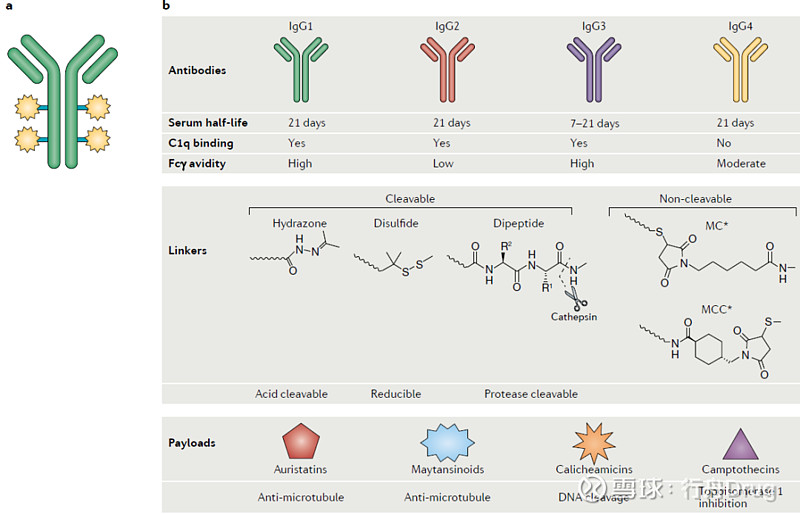
作用机制:干扰HER-2的自磷酸化,阻碍异二聚体的形成,抑制信号转导系统的激活,抑制肿瘤细胞的增殖。临床适应症1)适用于HER2过表达转移性乳腺癌;2)HER2过表达转移性乳腺癌接受过一种或多种化疗方案的单药治疗;3)联合紫杉醇或多西他赛,未接受过化疗的 HER2 过度表达转移性乳腺癌患者。用法用量 初始负荷剂量:本品推荐的初始负荷剂量为4mg/kg,静脉滴注90分钟以上。维持剂量:本品的推荐每周剂量为 2 mg/kg。如果初始负荷可以耐受,该剂量可在 30 分钟内静脉内给药。维持治疗直至疾病进展。乳腺癌辅助治疗:在完成所有化疗后开始使用曲妥珠单抗。曲妥珠单抗的初始负荷剂量为 8 mg/kg,随后每 3 周通过约 90 分钟静脉输注维持剂量为 6 mg/kg。总共使用了 17 剂(治疗 52 周)。用药注意事项(1)用药前检查HER-2是否过表达。不能使用5%葡萄糖溶液,因为它会引起蛋白质聚集。用无菌注射用水溶解配制本药,配制后的浓度为21mg/ml,使用前用生理盐水稀释。无菌注射用水含有苯乙醇作为防腐剂,对新生儿和3岁以下儿童有毒。本品不能用于静脉注射。使用注意事项(2)用药期间出现左心功能不全应停药。
与曲妥珠单抗治疗相关的充血性心力衰竭可能非常严重,尤其是与蒽环类药物和环磷酰胺联合使用时,但大多数症状会随着治疗而改善。治疗通常包括利尿剂、强心苷和/或 ACE 抑制剂。10% 的患者发生急性超敏反应,可通过抗组胺药、抗炎药和皮质类固醇来预防。西妥昔单抗()——抗EGFR单克隆抗体于2004年2月26日上市。它是一种表皮生长因子受体(EGFR)IgG1单克隆抗体,一种人和小鼠EGFR单克隆抗体。嵌合体由鼠抗 EGFR 抗体和人 IgG1 重链和轻链的恒定区组成。作用机制:与EGFR有很强的亲和力,能阻断生长因子的结合位点,防止配体诱导的受体活化和磷酸化,抑制酪氨酸激酶活化,阻断与肿瘤细胞增殖相关的信号转导。通路,抑制细胞增殖,抗血管生成和转移,促进细胞凋亡。临床适应症(1)2004年2月26日,美国FDA批准西妥昔单抗联合伊立替康治疗EGFR阳性、伊立替康无效或耐药复发或转移性直肠癌,或单药治疗不能耐受化疗的结直肠癌(2)美国FDA也批准西妥昔单抗联合放疗作为局部晚期头颈部鳞癌的一线治疗药物。(3)爱必妥于2007年在中国成功上市,用于治疗局部晚期头颈部鳞状细胞癌。)治疗以上两种疾病。西妥昔单抗是唯一被发现能够逆转化疗耐药的靶向药物。推荐起始剂量为/m2,输注时间120分钟,滴速控制在5ml/min以内。
维持剂量为1周/m2,输注时间不少于60分钟。在第一次输注该产品之前,患者必须接受抗组胺药治疗。建议患者在每次后续使用本产品前不要摇晃或稀释。使用注意事项 使用前应进行过敏试验。阳性者慎用,阴性者不能完全排除严重过敏反应的发生。本药不宜静脉注射、摇动或稀释。输液必须使用 0.2 um 或 0.22 um 微孔过滤器进行过滤。输液管必须在输液结束时用 0.9% 氯化钠注射液冲洗。此类患者在治疗期间应避光。轻度至中度皮肤毒性无需调整剂量。如果发生严重的皮肤毒性,应酌情减少剂量。当出现轻中度输液反应时,可减慢输液速度或服用抗组胺药。如出现严重输液反应,应立即停止输液,静脉给予肾上腺素、糖皮质激素、抗组胺药和支气管扩张剂。和氧疗。(二)各类概述及代表性药物介绍2、小分子酪氨酸激酶抑制剂1980年,等人首次发现并鉴定了RNA肿瘤病毒(RSV)感染的细胞转化基因产物,即酪氨酸激酶(TK)酪氨酸激酶与肿瘤的发生发展密切相关。超过 50% 的原癌基因和癌基因产物具有蛋白酪氨酸激酶活性。它们的异常表达可直接导致肿瘤进展。此外,该酶还与肿瘤转移、血管生成和肿瘤对化疗的耐药性有关。
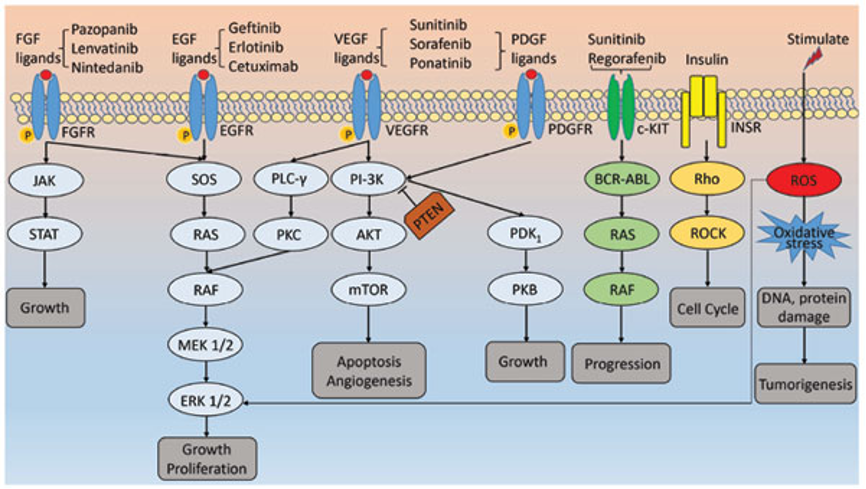
酪氨酸激酶抑制剂的研究是目前抗肿瘤药物研发的热点。蛋白酪氨酸激酶是信号转导中的关键酶之一,它催化三磷酸腺苷(ATP)的磷酸基团转移到底物蛋白的酪氨酸残基上并使其磷酸化。信号转导通路作用于一系列底物蛋白,产生多种生物学效应,调节细胞生长、分化、粘附、运动和死亡,并与包括肿瘤在内的多种人类疾病相关。在人类基因组中,PTK家族包含90个不同的TK,分属于30个亚科,其中20个亚科58个为受体型,10个亚科32个为非受体型。表皮生长因子受体(EGFR)简介 EGFR-TK是RTK家族的成员,其介导的细胞信号通路在肿瘤的形成和发展中发挥着重要作用。EGFR-TK在许多不同的实体瘤患者中过度表达,导致细胞生长不受控制,并且通常与预后不良、放化疗耐药、肿瘤血管生成和肿瘤转移有关,已成为肿瘤治疗的理想靶点。2002年至2009年,10个抗肿瘤激酶抑制剂在美国和欧洲获批上市,占同时获批的30个抗肿瘤新药的三分之一。抑制剂的化学结构不同,细胞内信号通路的抑制靶激酶也不同。第一代酪氨酸激酶抑制剂,如厄洛替尼,其抗表皮生长因子酪氨酸激酶抑制作用已得到临床研究的支持。但在临床应用中发现此类药物的有效率仅为9%-18%,且会引起肿瘤细胞的耐药性。
因此,单一靶点的抑制往往无法达到预期的治疗效果。细胞内的信号转导是一个复杂的、多因子的跨蛋白网络系统,上游信号因子与下游生物效应之间存在多条通路。. 为此,目前的研发重点主要是多靶点酪氨酸激酶抑制剂。多靶点药物可以抑制多个信号通路或通路中的多个分子。大量临床研究证实,此类药物对单靶点抑制剂耐药的肿瘤有效。近年来,美国FDA先后批准了五种低分子多靶点奶酪,伊马替尼()、索拉非尼()、舒尼替尼()、拉帕替尼()和达沙替尼()。列出了氨基激酶抑制剂。目前市场上的EGFR抑制剂作用机制及其结构EGF/TGFα?--?细胞(抗)/sR,代表伊马替尼(格列卫)的临床应用 2001年5月10日,美国FDA批准伊马替尼用于用错位的 Bcr-Abl 基因治疗慢性粒细胞白血病 (CML)。
2002年2月,美国FDA批准伊马替尼用于治疗胃肠道间质瘤(GIST)。该药物是靶向治疗最成功的例子。伊马替尼的可能作用机制 伊马替尼 c-Kit 受体细胞膜阻断 ATP 结合 伊马替尼应用前 ATP 结合受体激酶 部分信号转导通路被抑制 信号转导通路激活 细胞核 临床适应症1)用于无法切除和/或转移性恶性胃肠道间质瘤 (GIST);2)适用于纯素治疗失败后的慢性粒细胞白血病 (CML) 急变期、加速期或 α 干扰慢性期患者。剂量和给药起始剂量:慢性粒细胞白血病急变期和加速期患者甲磺酸伊马替尼的推荐剂量为/天;对于干扰素治疗失败的慢性期患者,以及不能切除或有转移的患者,对于恶性胃肠道间质瘤(GIST)患者,推荐剂量为 400 mg/d,均每天口服一次。建议随餐服用药物,只要有效就继续服用。剂量调整如果血细胞计数允许且无严重药物不良反应,剂量可从/天增加到/天,或从/天增加到/天(,分2次次)在以下情况下服用):疾病进展,治疗至少 3 个月后未能获得令人满意的血液学反应,并重新消除获得的血液学反应。下列情况必须调整剂量:治疗过程中如出现严重的非血液学不良反应(如严重的水潴留),应停药至不良反应消失,然后根据严重程度调整剂量的不良反应。
发生严重肝毒性时调整剂量:胆红素升高超过正常范围上限3倍或转氨酶升高超过正常范围上限5倍,应停药至上述指标分别降至正常范围上限1.5或2.5次以下。中性粒细胞或血小板减少症的剂量调整1)加速期或急变期:如果发生严重的中性粒细胞减少症和血小板减少症,建议将剂量减少至 400 毫克/天。如果血细胞连续减少 2 周,则进一步减少剂量至 300 毫克/天。若血细胞连续下降4周,应停药至中性粒细胞≥1.0×109/L,血小板≥20×109/L。重复使用的剂量为 300 毫克/天。2)α-干扰素治疗失败后的慢性期患者:中性粒细胞
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话