欢迎光临吉康旅!
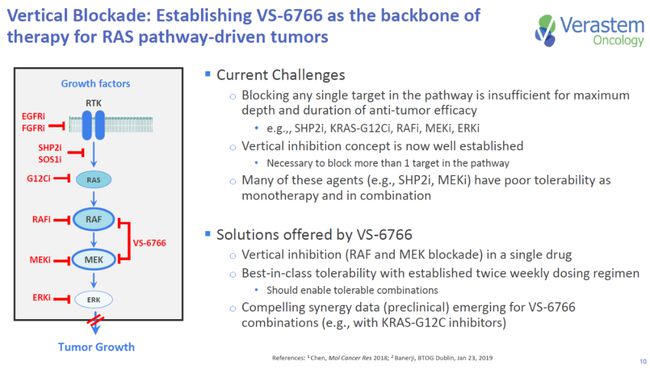
随着精准医学和基因检测技术的发展,越来越多的基因被发现和相关,其中鼠肉瘤病毒癌基因同源物B1(v-raf-coma B1,BRAF)基因可能是另一个重要的驱动基因[5] . NCCN 指南建议将其作为常规筛查的有效目标。此外,BRAF 和 MEK 抑制剂的组合已成为突变患者的护理标准。然而,非突变肺癌患者仍采用无驱动基因的治疗方案,缺乏有效的靶向治疗策略。免疫检查点抑制剂(ICIs)是目前驱动基因野生型肺癌的另一种重要治疗方法。目前研究表明,ICI对BRAF阳性患者的治疗具有部分获益。
1 BRAF基因概述
1.1 BRAF基因的生物学特性
BRAF基因是重要的原癌基因,位于7号染色体,有18个外显子,编码BRAF蛋白,与A-RAF和C-RAF同属RAF家族,是RAS-RAF-MEK-ERK通路。丝裂原活化蛋白激酶 (-, MAPK) 的上游调节剂,在调节细胞生长和繁殖中起重要作用。MAPK通路的异常信号主要是由RAS和BRAF突变引起的。当突变发生时,BRAF 蛋白磷酸化并持续激活下游的细胞外调节激酶 (, ERK),最终导致肿瘤发生。所有 RAF 蛋白都会使 MEK 磷酸化,但 BRAF 具有最高的激酶活性。
一个常见的突变是在氨基酸 600 处用缬氨酸 (V) 取代谷氨酸 (E),使 BRAF 作为结构活性单体发挥作用;教授在 2020 年美国临床肿瘤学会 (ASCO) 年会上的报告表明,同时具有 KRAS G13C、cMET 14 跳跃和其他共突变的 BRAF 突变患者接受靶向治疗也显示出疗效。
1.2 BRAF突变的临床特征
BRAF基因突变是一种广谱基因突变,最早发现于人类尤文氏肉瘤,恶性实体瘤的发病率约为7%,恶性黑色素瘤的发病率约为50%,甲状腺乳头状癌的发病率为36%——53%,散发性结直肠癌为5%-22%,低级别卵巢浆液性癌约为30%。肺癌中BRAF突变的检出率为1%-3%。肺腺癌较为常见,不同国家、不同种族无明显差异。突变和非突变各占 BRAF 突变肺癌的 50%。
一项回顾性研究分析了 1837 例 EGFR 突变患者的临床和分子特征,发现在相同驱动基因的患者中,不同的突变亚组可能具有不同的临床特征,他们从相同治疗中获益的程度可能存在差异. 另一项对 1,046 名患者的回顾性研究发现,BRAF 突变型肺癌患者多为女性,不吸烟,80% 的突变型肿瘤具有微乳头特征,与较短的无病生存期(-,DFS)显着相关总生存期( ,OS),非突变患者有吸烟史,与预后无显着相关性。回顾性研究表明,与未突变的 BRAF 相比,突变与预后不良有关,
1.3 BR AF 突变的检测
目前NCC N指南推荐的BRAF突变检测方法包括测序、实时聚合酶相关反应(RT-PCR)和二代测序(nex,NGS)。测序属于二代测序,主要用于点突变和小突变突变。可检测V600突变和罕见突变,但灵敏度低,无法检测染色体拷贝数和易位的变化,肿瘤细胞含量较高(>20%)。RT-PCR是一种可以检测已知突变的靶向方法。检测限低,可检测7%的突变DNA拷贝数,价格低廉,灵敏度为97.5%。检出率较高,主要缺点是经常遗漏罕见的 BRAF 突变亚型。NGS 支持同时进行多基因检测,包括所有可能的变异类型,例如突变、插入和扩增,DNA 检测下限为 5%,从而使更广泛的分子谱能够识别患者可能接受靶向治疗的其他稀有基因驱动突变的缺点是需要很长时间。免疫组织化学 (IHC) 是检测 BRAF 突变的另一种选择方法。最常用的抗体是单克隆抗体VE1,它具有很高的灵敏度和特异性,还可以检测所有非突变的BRAF。100%。它的主要缺点是由于 BRAF 的高异质性或低丰度而可能出现假阴性,并且目前缺乏针对 BRAF 或其他变体的抗体,该诊断测试无法确定其他突变的存在。还,因为 IHC 识别蛋白质而不是 DNA,所以 IHC 和基于 DNA 的检测结果之间可能存在差异。上述检测方法均以组织活检为基础,但液体活检近年来发展迅速,已成为许多无法获取组织样本的患者的替代方法。然而,由于血液缺乏解剖特异性,并且血液中存在 BRAF 突变的 DNA 并不能表明肿瘤的数量或肿瘤的起源,因此液体活检的局限性仍然存在。
2 BRAF突变的靶向治疗
BRAF阳性患者的靶向治疗药物主要包括BRAF抑制剂和MEK抑制剂。以往的研究发现,两种靶向药物的联合治疗比单一药物更有效。
2.1 BRAF 抑制剂
2.1.1 威罗非尼 ()
威罗非尼是BRAF的选择性抑制剂,能有效抑制BRAF的活性。Drug, FDA) 批准用于治疗具有突变的不可切除或转移性恶性黑色素瘤。威罗非尼抗肿瘤活性的第一个确凿证据来自对 BRAF 阳性非黑色素瘤癌症的一揽子研究。在这项研究中,接受威罗非尼单药治疗的 19 名 BRAF 阳性治疗经验患者队列在第 8 周达到了 42% 的客观缓解率 (ORR) 和 7.3 个月的中位 PFS,即 12 个月的 OS为 66%。研究结果达到了预先设定的终点,队列扩大到总共 62 名患者,包括 54 名接受过治疗的患者和 8 名未接受过治疗的患者 [36]。平均 10.7 个月随访后,ORR 为 37. 0% (95%CI: 24.3%-51.3%) 在既往治疗的患者中,中位 PFS 为 6.1 个月,中位 OS 达到 15.4 个月。初治患者的 ORR 为 37.5% (95%CI:8.5% -75.5%),中位 PFS 为 12.9 个月,中位 OS 不成熟,最常见的不良反应是恶心(40%)。 使一线治疗初治患者的 PFS 翻了一番。
在一项回顾性队列研究中,共有 35 名晚期 BRAF 突变患者(包括 29 名突变和 6 名非突变)接受了不同 BRAF 抑制剂的治疗,包括威罗非尼、达拉非尼或索拉非镍。31 名患者接受了一种 BRAF 抑制剂,4 名患者在前后接受了两种抑制剂。接受BRAF单药靶向治疗的患者ORR为53%(95%CI:35.1%-70.2%),疾病控制率(rate,DCR)为85 % (95%)。%CI:68.9%-95.0%)。在接受威罗非尼治疗的 24 名可评估患者中,ORR 为 54%(95%CI:32.8%-74.4%),DCR 为 96%(95%CI:7< @8.9%-99.9%)。总体人群中位 PFS 为 5 个月,OS 为 10.8 个月;
法国国家癌症研究所进行的威罗非尼篮子试验,旨在评估威罗非尼在 BRAF 阳性实体瘤中的疗效和安全性。该队列共有 118 名患者,其中 101 名突变,17 名 BRAF 非 V600 突变,97、2、1 和 1 名 BRAF V600 突变,中位随访时间为 23.9 名患者。在 BRAF 非 V600 队列中,未观察到客观反应,队列停止。在 BRAF V600 队列中,ORR 为 44.9%,中位 PFS 为 5.2 个月(95%CI:3.8-6.8), OS 为 10 个月(95%CI:6.8-15.7)。以上所有研究表明,BRAF 突变肺腺癌患者的预后比非突变患者,受益于靶向治疗。
2.1.2 达拉非尼 ()
是一种可逆的 BRAF 激酶抑制剂,通过抑制失控的 BRAF 蛋白来抑制肿瘤生长。达拉非尼对 BRAF 突变患者的疗效最初是在一项纳入 BRAF 突变实体瘤患者的 I 期试验中发现的。该研究中唯一的 BRAF 突变患者对该治疗有反应,后来在一项全球研究中发现其与威罗非尼的作用相似,该研究于 2013 年被 FDA 批准用于治疗 BRAF 突变黑色素瘤。
在教授发起的 II 期临床研究中,84 名 BRAF V600 突变患者接受了单药达拉非尼治疗,其中 78 名接受过治疗的患者和 6 名初治患者。结果显示,的ORR为33%,DCR为58%,中位PFS为5.5个月,中位OS为12.7个月。84 名患者中有 35 名(42%)发生了严重的不良事件,但大多数是可以耐受的。这项II期临床研究表明,达拉非尼单药治疗对BRAF阳性患者具有一定的抗肿瘤活性,但治疗效果有限。
2.2 达拉非尼联合用药
BRAF抑制剂单药的耐药机制可能与MAPK通路的重新激活有关。如果在BRAF抑制剂中加入MEK抑制剂,可能会阻断ERK信号通路,从而延长患者的疾病控制时间。达拉非尼组合在治疗 BRAF 突变患者中显示出协同作用。
这是一项单独或联合曲美替尼治疗 BRAF 突变经历或初治患者的 II 期临床研究。该研究分为三个队列:队列 A 是达拉非尼单药治疗组,队列 B 是接受过治疗的患者组,联合达拉非尼和曲美替尼,队列 C 是未接受过联合治疗的患者组。
@7.0-16.6),中位OS为24.6个月,ORR达到64%。与单药 BRAF 靶向治疗相比,双靶点组合在 BRAF 突变患者的一线和后线治疗中均显示出益处。基于此,2017年FDA批准了BRAF-MEK双靶点疗法,用于BRAF突变晚期患者。
在法国进行的 GFPC 真实世界研究包括 40 名既往接受过治疗或未经治疗的晚期 BRAF 突变患者,他们接受了达拉非尼联合曲美替尼治疗。结果显示,中位 PFS 和 OS 分别为 17.5 个月(95%CI:7.1-23.0) 和 25.5个月(95%CI:16.6-未达到)。接受一线治疗的 9 例患者的中位 PFS 为 16.8 个月(95%CI:6.1 -23.2),中位OS为21.8个月(95%CI:1.0-未达到),31例接受二线及以上治疗患者中位 PFS 和 OS 分别为 16.8 个月(95%CI:6.1-23.2) 和 25.5 个月,分别为(95 %CI:16.6-未达到),
在一项针对中国患者的回顾性研究中[41],共纳入 65 例患者,其中 54 例有突变,11 例无突变。在接受 BRAF 抑制剂治疗的 30 名突变患者中,单独使用 、单独使用 和 联合曲美替尼的中位 PFS 分别为 7.8 个月和 6 个月(P=0.970). 对于一线化疗,中位 PFS 与非患者相似(5.4 个月 vs. 5.4 个月,P=0.82 5).本研究提示BRAF靶向治疗对中国BRAF突变患者具有临床获益。
2.3 其他新药
(BGB-232),一种 RAF 家族关键激酶和 EGFR 的新型抑制剂,正在 1 期临床试验中评估其在 BRAF V600 突变实体瘤中的疗效。在这项 1 期研究中,在 53 名 BRAF 患者中-突变实体瘤,8例(15.1%)部分缓解(,PR),27例(50.9%)疾病稳定(,SD)。对BRAF V600突变实体瘤患者的治疗有一定的获益,但需要进一步研究单药或联合用药的安全性和有效性。目前MEK抑制剂联合治疗的I/II期试验BRAF 突变的实体瘤 () 已经启动。
所有 BRAF 突变均激活 ERK 磷酸化,因此推测受 ERK 信号通路调节的转录因子是 BRAF 突变的潜在下游靶点,对 BRAF 和 MEK 抑制剂的获得性耐药可能与 MAPK 信号通路中 ERK 的重新激活有关。临床前证据还发现,小分子 ERK 抑制剂可以延缓耐药性的出现。在一项多中心 I 期剂量递增和扩展临床试验中,共有 91 名 BRAF 基因突变患者,ERK 激酶抑制剂在 BRAF V600 和非 V600 突变实体瘤中均显示出抗肿瘤活性,其中 28 50% 的患者BRAF 非 V600 突变有客观反应。这项研究提供了第一个临床证据表明 BRAF 非 V600 突变可能通过下游 ERK 抑制起作用,
磷脂酰肌醇3-激酶/蛋白激酶B/雷帕霉素靶蛋白(-/B/, PI3K/AKT/mTOR)通路参与多种实体瘤的发生发展,包括黑色素瘤、乳腺癌、结肠癌等。 ,可能是对 BRAF-MEK 靶向治疗产生获得性耐药的机制之一。PX-866 是一种不可逆异构体 PI3K 抑制剂,与 BRAF 抑制剂联合使用时,对黑色素瘤细胞系的增殖具有协同抑制作用。Yam 等人在晚期 BRAF V600 突变肿瘤患者中对 PX-866 和 的组合进行了多中心 I 期研究,以确定 PX-866 和 组合的安全性。由于本研究没有招募 BRAF 突变的患者,联合治疗对此类患者的疗效尚不清楚,
3 BRAF 突变的免疫治疗
在驱动基因阳性的患者中,ICIs的活性比较弱,在未选择的患者中有效率为14%-20%。因此,免疫治疗对驱动基因阳性肺癌患者的疗效仍处于探索阶段,免疫治疗对BRAF突变患者的疗效尚不明确。
这是对免疫疗法在晚期驱动基因阳性患者中疗效的回顾性分析。该研究纳入了551名各类驱动基因阳性肺癌患者,其中BRAF队列中的43名患者,治疗线数中位数为二线,程序性细胞死亡受体配体1(1,PD-L1)中位表达水平为50%,ORR为24%,中位PFS为3.1个月,中位OS为13.6个月。患者疗效有限,无统计学差异与其他 BRAF 突变的生存获益。
2020年在中国开展的一项多中心回顾性研究,收集了4178例患者的免疫治疗信息,探讨免疫治疗对BRAF突变患者的疗效。在BRAF突变体和BRAF野生型亚组分析中,野生型PD-L1的表达高于突变体(P=0.198),而突变体中的TMB高于野生型(P=0.198))。=0.009),但两组的 OS 没有差异(P=< @0.334).进一步分析发现BRAF非组的中位OS远高于组(14个月vs 5个月),并达到统计学差异(P=0. 017)。
总之,与未选择的患者相比,靶向治疗耐药的 BRAF 突变患者的二线或后线治疗中免疫治疗的疗效没有显着差异。BRAF突变患者在一定程度上受益于免疫治疗,但非常有限。
4 勘探与展望
目前,BRAF抑制剂联合MEK抑制剂是治疗晚期BRAF突变患者最有效的策略,不受治疗线数的影响。对于靶向治疗耐药的患者,免疫治疗有一定疗效,但获益有限,双靶点联合免疫治疗尚处于研究探索阶段。
尽管靶向治疗取得了显着的疗效,但大多数患者的耐药性仍是不可避免的。目前关于黑色素瘤获得性耐药机制的研究较多,BRAF靶向药物在患者中的耐药机制尚未完全阐明。在对 BRAF 抑制剂耐药的黑色素瘤患者中检测到 PTEN 缺失,而 PTEN 缺失的患者接受 BRAF 抑制剂的 PFS 较短,这可能表明 PTEN 缺失与对 BRAF 抑制剂的原发性耐药有关。相关研究报道,BRAF突变患者对靶向治疗产生耐药性,涉及出现KRAS G12D、KRAS G12V或突变,而原有的BRAF驱动突变并未消失。所以,RAS抑制剂联合BRAF抑制剂双靶点治疗可降低耐药风险。发生可能是一个新的研究方向。此外,BRAF突变也被发现是第三代TKI奥希替尼的耐药机制之一,有EGFR突变对奥希替尼耐药的患者接受达拉非尼、曲美替尼和奥希替尼三靶点治疗的病例报道。获得了13.4个月的临床反应,但其安全性和有效性仍需大样本的后续研究。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话