欢迎光临吉康旅!
2017年9月23日,美国食品药品监督管理局(FDA)批准索拉非尼用于肝癌患者,标志着肝癌免疫治疗时代的正式到来。在之前的文章中,抗癌医生曾经向癌症朋友介绍过肝癌免疫治疗的概况(肿瘤科医生会带你了解肝癌的免疫治疗)。
今天,在整理完盘点后,抗癌医生将为大家详细介绍2017年底以PD-1抑制剂为代表的肝癌领域最新研究成果。
癌症医生将从以下几个方面进行讲解:
1PD-1抑制剂单用治疗原发性肝癌的研究现状
早在2015年ASCO会议上,相关研究人员就公布了PD-1抗体治疗晚期HCC的I/II期临床结果,这也为PD-1抑制剂治疗晚期肝癌的后续研究奠定了基础。肝癌。
在探索PD-1抑制剂治疗肝癌的安全剂量试验中,研究人员发现HCV和HBV感染(乙肝和丙肝患者)的安全剂量为3mg/kg。对于无肝炎病毒感染者,安全剂量为10mg/kg。
该研究以47例晚期原发性肝癌患者为研究对象,70%有肝外转移,13%有血管侵犯,68%有索拉非尼治疗史。截至中期分析节点,17例患者仍在接受治疗,26例因疾病进展停药1例,因不良反应停药2例,因CR停药2例。
在不良反应方面,唯一的IV级不良反应是IV级脂肪酶水平升高。此外,5 名患者 (11%) 的 AST 升高,4 名 (9%) 的 ALT 升高。人们之前担心的自身免疫性疾病和肝功能障碍并没有出现。
短期疗效方面,肿瘤完全消失(CR)2例,占治疗总人数的5%;6例患者肿瘤明显缩小(PR),占14%;肿瘤没有继续生长(SD)20例,占48%;其余14例患者无效(PD),占33%。
同时,研究结果还显示,在HBV感染组、HCV感染组和无病毒组中,均存在肿瘤缩小的患者。对于对治疗有反应的患者,效果是持久的(这与靶向治疗不同,因为大多数对靶向治疗有反应的患者在治疗一段时间后会产生耐药性,让肿瘤复发或转移)。该研究指出,用 PD-1 抗体治疗 HCC 患者会产生持久的反应,这是免疫检查点抑制剂最独特和最显着的特点。
在上述研究的基础上,研究人员确定剂量为3 mg/kg,并将样本量扩大到214例。结果显示,在所有研究对象中,CR为2例(1%),PR为33例(15%),SD 111例(52%),PD 63例(29%)。9个月生存率为70%。副作用方面,3-4级AST升高率为4%,3-4级ALT升高率为3%。病毒性肝炎患者使用后无严重肝功能障碍。这表明PD-1抑制剂在肝癌患者的治疗中是安全的。
为了进一步观察PD-1抑制剂治疗肝癌的临床效果,目前全球范围内正在进行更深入的III期临床研究。这样大规模的研究主要有两个,一个是直接对比索拉非尼一线治疗晚期原发性肝细胞癌的临床研究;另一项针对 HCC 的研究表明,与安慰剂相比,索拉非尼对二线治疗(药物 K)没有反应,其结果尚未报告。
此外,CTLA-4抑制剂治疗HCC的研究也在进行中,但初步结果发现其副作用比PT-1抗体多。不仅如此,抗PD-1/PD-L1抗体与抗CTLA-4抗体联合治疗晚期HCC的I/II期研究也已启动,结果也值得期待到。
2PD-1抑制剂联合其他免疫治疗药物治疗肝癌的研究进展
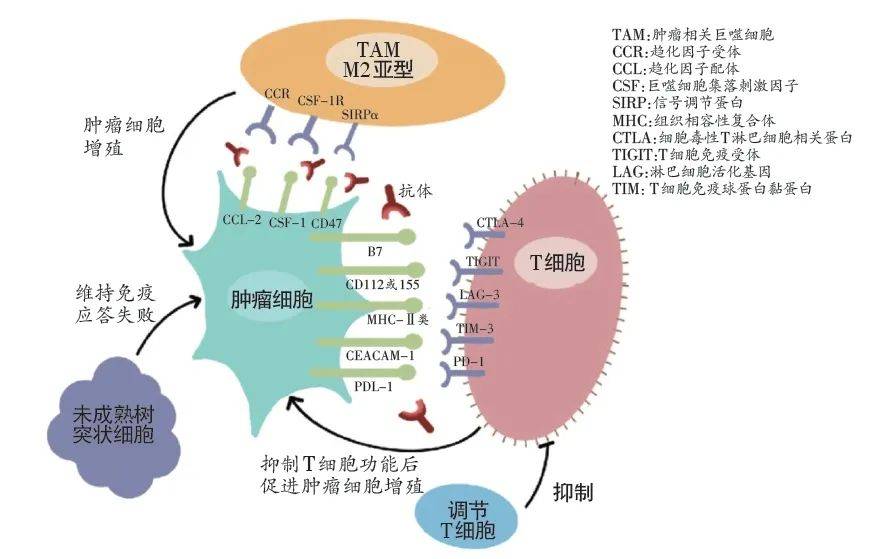
在之前的文章中,抗癌医生已经详细介绍了当前免疫治疗药物的种类及其抗肿瘤机制。总之,目前的免疫治疗药物主要是PD-1/PD-L1抑制剂和CTLA-4抑制剂(肿瘤科医生带你了解“免疫检查点抑制剂”如何治疗恶性肿瘤)。
这两种药物中的一种可以阻断免疫细胞与肿瘤细胞的内在联系,让免疫细胞识别并杀死肿瘤细胞(PD-1/PD-L1抑制剂),另一种可以大量增加免疫细胞。数(CTLA-4抑制剂),两药联合治疗恶性肿瘤有协同作用。
这种联合治疗的基本原理是,当肿瘤中不存在靶淋巴细胞(CD8+ T 细胞)时,抑制 PD-1 和 PD-L1 通路无法刺激癌症免疫微环境。然而,同时使用抗CTLA-4抗体可确保抑制B7-CTLA-4通路,导致淋巴结CD8+ T细胞增殖并浸润至肿瘤组织,从而增强抗肿瘤作用。此外,肿瘤微环境中的抗CTLA-4抗体可以抑制表达表面CTLA-4的Treg细胞的抑癌作用。
该联合疗法目前正在进行肝癌治疗领域的I/II期临床试验。I期试验数据已公布,40例原发性肝细胞癌患者和20例无病毒感染患者的客观缓解率为25%。有效率为40%。二期实验数据将于2018年4月发布。
可见,两种免疫治疗药物联合治疗肝癌的临床数据并不十分丰富,还需要进一步的临床试验数据积累。
3PD-1抑制剂与其他抗肿瘤疗法的组合
原发性肝细胞癌的治疗方法很多,除手术治疗外,还包括介入治疗、消融治疗、放射治疗、靶向治疗等。
初步临床探索发现,放疗和其他局部治疗(如经导管动脉化疗栓塞和射频消融)可以通过诱导局部炎症和释放抗原来激活免疫系统,提高PD-1抗体的疗效。
研究表明,放射治疗、TACE 和 RFA 通过释放肿瘤相关抗原并刺激细胞毒性 T 淋巴细胞向肝内转移性小结节迁移来诱导肿瘤免疫原性。因此,后续使用抗PD-1抗体可以控制这些小的肝内转移结节。
在一项研究中,RFA 显着增加了 62% 患者的肿瘤抗原特异性 T 细胞数量,证实了肿瘤相关抗原的释放。该研究还表明,与肿瘤抗原特异性 T 细胞水平低的患者相比,肿瘤抗原特异性 T 细胞水平高的患者的无复发生存率显着提高。
关于放疗联合免疫治疗的介绍,抗癌医生在之前的文章中已经多次提及和阐述,在此不再赘述(放疗——肿瘤免疫治疗的“理想搭档”)。
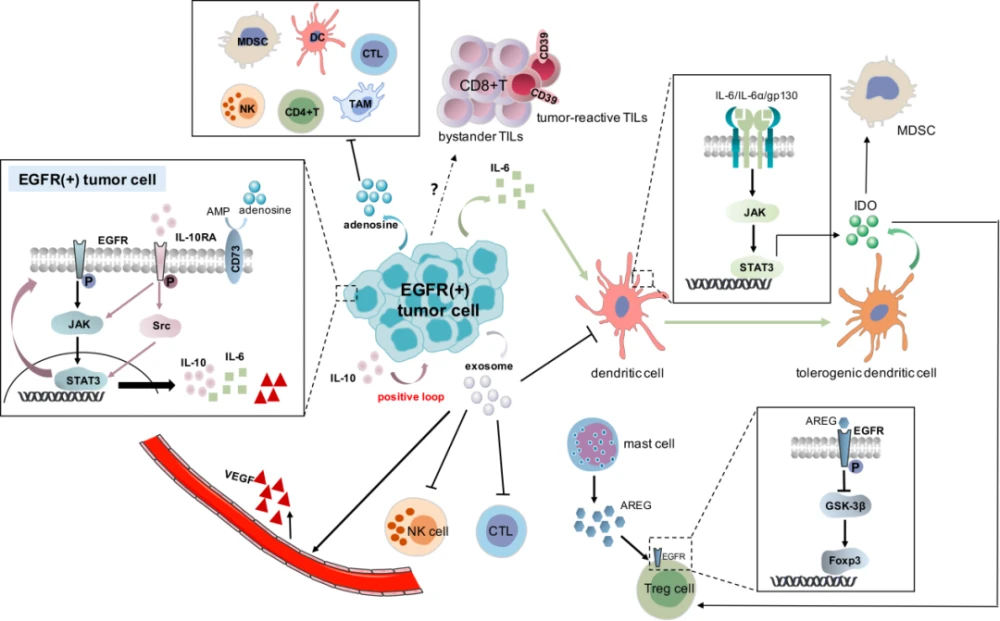
在肝脏微环境中,具有免疫抑制作用的细胞包括肝间质细胞中的枯否细胞、树突状细胞、内皮细胞和肝星状细胞,以及白细胞介素(IL)-10和转化生长因子(TGF)-β等免疫抑制细胞因子。和 PD-1/PD-L1 通路。这种免疫抑制环境可以通过分子靶向药物和免疫检查点抑制剂的组合来改变。
以下是目前正在进行的多种靶向联合免疫疗法的临床试验,结果值得期待。其中,日本正在进行乐伐替尼联合K药的I期临床试验。具体实验设计如下:
在临床前基础研究中,通过抑制肿瘤相关巨噬细胞和 Treg 诱导的癌症免疫抑制环境,降低 TGF-β 和 IL-10、PD-1 表达和 Tim-3 的表达水平,从而触发免疫刺激细胞因子等介导的抗癌免疫作为 IL-12。
这些基础研究可为寻找适合免疫检查点抑制剂的分子靶向药物提供参考。可以说,目前免疫治疗与靶向治疗联合治疗原发性肝细胞癌的研究还处于起步阶段。控制概率,临床应用前景十分广阔。
4年来,以PD-1抑制剂为代表的肿瘤免疫治疗犹如一股春风,吹遍了恶性肿瘤治疗领域。对于传统治疗控制不佳的原发性肝癌,免疫疗法为其开辟了新的机遇。一种全新的治疗方式。
目前,以免疫治疗为核心的综合运用多种治疗模式的临床试验已在肝癌治疗领域广泛开展。相信随着临床经验的不断丰富,肝癌将从一种无法治愈的疾病转变为部分治愈的疾病。患者的春天将伴随着免疫疗法的发展而来。
癌症医生 2018 年 3 月
上一期癌症快报案例分析:火凤凰治疗案例
基本情况:火凤凰,女,47岁,腺癌IV期,脑转移瘤,骨转移瘤;EGFR 21 突变,ALK 阴性。
讨论:
1.患者的治疗经验和教训;
2.关于未来治疗方案的讨论;
点击“查看”观看精彩内容~
查看
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话